解答题-结构与性质 适中0.65 引用1 组卷80
(1)钛铁合金具有吸氢特性,工业在制造以氢为能源的热泵和蓄电池等方面有广阔的应用前景,金属Ti(六方最密堆积)的原子空间利用率约为_______ ,基态Ti原子核外有_______ 个运动状态不同的电子,在基态Ti2+中,电子占据的能量最高的轨道为_______ 。
(2)已知Si-Si键能为176 kJ/mol,Si-O键能为460 kJ/mol,O=O键能为497.3 kJ/mol,则可计算出1 mol硅与足量氧气反应时将放出_______ kJ的热量。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般为d0或d10排布时,无颜色;为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色,据此判断 [Mn(H2O)6]2+_______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。COCl2分子的空间构型为_______ ;Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______ 。
(5)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(如图),则该晶体中镁、碳、镍三种元素的原子个数比是_______ ,晶体中每个镁原子周围距离最近的镍原子有_______ 个。
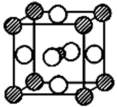
(图中:碳原子用小 球在晶体的体心,镍原子用大
球在晶体的体心,镍原子用大 球,镁原子用大
球,镁原子用大 球)
球)
(2)已知Si-Si键能为176 kJ/mol,Si-O键能为460 kJ/mol,O=O键能为497.3 kJ/mol,则可计算出1 mol硅与足量氧气反应时将放出
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般为d0或d10排布时,无颜色;为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色,据此判断 [Mn(H2O)6]2+
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。COCl2分子的空间构型为
(5)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(如图),则该晶体中镁、碳、镍三种元素的原子个数比是

(图中:碳原子用小
 球在晶体的体心,镍原子用大
球在晶体的体心,镍原子用大 球,镁原子用大
球,镁原子用大 球)
球)20-21高二下·福建福州·期中
类题推荐
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N元素的电负性由大到小的顺序是______ ,C60和金刚石都是碳的同素异形体,二者相比,熔点高的是______ ,原因是______ 。
(2)A、B均为短周期金属元素,依据表中数据,写出B的基态原子的电子排布式:______ 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,d0或d10排布无颜色,d1~d9排布有颜色。如[Co(H2O)6]2+显粉红色。据此判断:[Mn(H2O)6]2+______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为 ,每个COCl2分子内含有
,每个COCl2分子内含有______ 个σ键,______ 个π键,其中心原子采取______ 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)。反应过程中,断裂的化学键只有配位键,则形成的化学键类型是______ 。
(1)C、Si、N元素的电负性由大到小的顺序是
(2)A、B均为短周期金属元素,依据表中数据,写出B的基态原子的电子排布式:
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为
 ,每个COCl2分子内含有
,每个COCl2分子内含有②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)。反应过程中,断裂的化学键只有配位键,则形成的化学键类型是
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题。
(1)C、Si、N元素的电负性由大到小的顺序是___________________________ 。C60和金刚石都是碳的同素异形体,金刚石熔点高于C60熔点,原因是__________________________________________________________________________ 。
(2)A、B均为短周期金属元素。依据下表数据和已学知识,
写出B原子的电子排布式:___________________________ 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+_______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、络合物Fe(CO)5等。
①已知COCl2分子的结构式为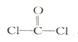 ,则 COCl2分子内含
,则 COCl2分子内含_______ (填标号)。
A.4个 键
键
B.2个 键、2个
键、2个 键
键
C.2个 键、1个
键、1个 键
键
D.3个 键、1个
键、1个 键
键
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是___________ 。
(1)C、Si、N元素的电负性由大到小的顺序是
(2)A、B均为短周期金属元素。依据下表数据和已学知识,
| 电离能/KJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
写出B原子的电子排布式:
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+
(4)利用CO可以合成化工原料COCl2、络合物Fe(CO)5等。
①已知COCl2分子的结构式为
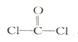 ,则 COCl2分子内含
,则 COCl2分子内含A.4个
 键
键B.2个
 键、2个
键、2个 键
键C.2个
 键、1个
键、1个 键
键D.3个
 键、1个
键、1个 键
键②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 ,与CN
,与CN


