填空题 适中0.65 引用1 组卷115
SO2是大气的主要污染物,工业上利用钠碱循环法可除去二氧化硫。回答下列问题:
(1)钠碱循环法中,吸收液为Na2SO3溶液,其水溶液在常温下pH__ 7(大于、小于、或者、等于)。
(2)可用Na2SO3溶液吸收SO2制备NaHSO3。该反应的离子方程式是___ 。
(3)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列各组微粒可以大量共存的是__ (填字母)。
A.CO 和HSO
和HSO B.HCO
B.HCO 和HSO
和HSO C.SO
C.SO 和HCO
和HCO D.H2SO3和HCO
D.H2SO3和HCO
(4)吸收液吸收SO2的过程中,水溶液中H2SO3、HSO 、SO
、SO 随pH的分布如图:
随pH的分布如图:
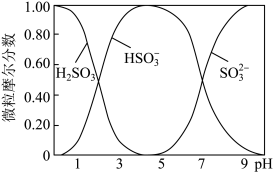
①在0.1mol/LNaHSO3溶液中离子浓度关系不正确的是____ (填字母)。
A.c(Na+)=2c(SO )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)
B.c(H+)-c(OH-)=c(SO )-c(H2SO3)
)-c(H2SO3)
C.c(Na+)>c(HSO )>c(SO
)>c(SO )>c(OH-)
)>c(OH-)
D.c(Na+)+c(H+)=2c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
②室温下,向一定量的漂白液(主要成分NaClO)中滴加适量的NaHSO3溶液,该过程中溶液pH的变化是___ 。写出该反应的离子方程式___ 。
(5)泡沫灭火器内外桶中各盛有一定浓度的NaHCO3、Al2(SO4)3溶液。使用时须将该灭火器反转并拔掉插销,让上述溶液混合并由喷嘴喷射出一定量的气流和难溶物,覆盖在可燃物的表面起到灭火效果。
①写出该反应的离子方程式___ 。
②泡沫灭火器可适合于扑灭下列哪种物品的初期着火___ 。(填序号)
A.植物油 B.金属镁粉 C.家用电器 D.棉纱纸张
(1)钠碱循环法中,吸收液为Na2SO3溶液,其水溶液在常温下pH
(2)可用Na2SO3溶液吸收SO2制备NaHSO3。该反应的离子方程式是
(3)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列各组微粒可以大量共存的是
A.CO
(4)吸收液吸收SO2的过程中,水溶液中H2SO3、HSO

①在0.1mol/LNaHSO3溶液中离子浓度关系不正确的是
A.c(Na+)=2c(SO
B.c(H+)-c(OH-)=c(SO
C.c(Na+)>c(HSO
D.c(Na+)+c(H+)=2c(SO
②室温下,向一定量的漂白液(主要成分NaClO)中滴加适量的NaHSO3溶液,该过程中溶液pH的变化是
(5)泡沫灭火器内外桶中各盛有一定浓度的NaHCO3、Al2(SO4)3溶液。使用时须将该灭火器反转并拔掉插销,让上述溶液混合并由喷嘴喷射出一定量的气流和难溶物,覆盖在可燃物的表面起到灭火效果。
①写出该反应的离子方程式
②泡沫灭火器可适合于扑灭下列哪种物品的初期着火
A.植物油 B.金属镁粉 C.家用电器 D.棉纱纸张
20-21高二上·贵州毕节·阶段练习
类题推荐
SO2是大气的主要污染物,工业上利用钠碱循环法可除去SO2。回答下列问题:
(1)除SO2的吸收液为Na2SO3溶液,该反应的离子方程式是__________ 。
(2)在0.1mol/L Na2SO3溶液中离子浓度关系不正确 的是__________(填字母)。
(3)泡沫灭火器内外桶中各盛有一定浓度的NaHCO3、Al2(SO4)3溶液。使用时须将该灭火器反转并拔掉插销,让上述溶液混合并由喷嘴喷射出一定量的气流和难溶物,覆盖在可燃物的表面起到灭火效果。
①该灭火器一般用塑料内桶盛装Al2(SO4)3的原因是(用离子方程式表示):__________ 。
②写出该灭火器灭火原理的离子方程式__________ 。
(1)除SO2的吸收液为Na2SO3溶液,该反应的离子方程式是
(2)在0.1mol/L Na2SO3溶液中离子浓度关系
| A. |
| B. |
| C. |
| D. |
①该灭火器一般用塑料内桶盛装Al2(SO4)3的原因是(用离子方程式表示):
②写出该灭火器灭火原理的离子方程式
(1)常温下,某水溶液M中存在的离子有Na+、A2-、HA-、H+、OH-,存在的分子只有H2O,根据题意回答下列问题。
①写出酸H2A的电离方程式:_____
②若溶液M由10 mL 2 mol∙L-1 NaHA 溶液与10 mL2 mol∙L-1 NaOH溶液混合而得,则溶液M的pH_______ (填“>”“<”或“=”)7,溶液M中各粒子的浓度关系正确的是____ (填序号)。
A.c(Na+)>c(A2-)>c(OH-)>c(H+)
B.c(HA-)+2c(H2A)+c(H+)=c(OH-)
C.c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+)
D.c(A2-)+c(HA-)=1mol∙L-1
(2)实验室可用NaOH溶液吸收NO2,,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1L溶液A,溶液B为0.1 mol∙L-1的CH3COONa溶液,则两溶液中c( )、c(
)、c( )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为____ (已知HNO2的电离常数Ka=7.1×10-4, CH3COOH的电离常数Ka=1.7×10-5)。可使溶液A和溶液B的 pH相等的方法是_____ (填序号)。
a.向溶液A中加适量水 b.向溶液A中加适量 NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(3)直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2.吸收液(NaOH溶液)吸收SO2的过程中,pH随n( ):n(
):n( )的变化关系如下表:
)的变化关系如下表:
①由上表判断 NaHSO3溶液显_______ 性。
②当吸收液呈中性时,溶液中离子浓度的大小关系为_______
①写出酸H2A的电离方程式:
②若溶液M由10 mL 2 mol∙L-1 NaHA 溶液与10 mL2 mol∙L-1 NaOH溶液混合而得,则溶液M的pH
A.c(Na+)>c(A2-)>c(OH-)>c(H+)
B.c(HA-)+2c(H2A)+c(H+)=c(OH-)
C.c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+)
D.c(A2-)+c(HA-)=1mol∙L-1
(2)实验室可用NaOH溶液吸收NO2,,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1L溶液A,溶液B为0.1 mol∙L-1的CH3COONa溶液,则两溶液中c(
a.向溶液A中加适量水 b.向溶液A中加适量 NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(3)直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2.吸收液(NaOH溶液)吸收SO2的过程中,pH随n(
n( | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
②当吸收液呈中性时,溶液中离子浓度的大小关系为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



