单选题 较易0.85 引用2 组卷304
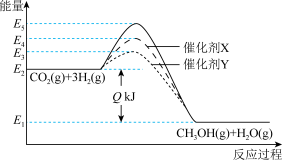
已知: 。不同情况下反应过程的能量变化如图。下列结论正确的是
。不同情况下反应过程的能量变化如图。下列结论正确的是

| A.1mol |
| B.催化剂可以改变反应途径,缩短达到平衡的时间 |
| C.当生成的水为液态时,Q值减小 |
| D.催化剂不同,反应的热效应不同 |
2021·上海浦东新·二模
类题推荐
以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图所示。下列叙述正确的是
的过程如图所示。下列叙述正确的是


| A.过程中 |
| B.该过程的热化学方程式可以表示为: |
| C.过程II中3 |
| D.铁氧化合物循环制 |
通过以下反应均可获取H2。下列有关说法正确的是
①焦炭与水反应制氢:C(s)+ H2O(g) = CO(g)+ H2(g) ΔH1 = 131.3 kJ·mol–1
②太阳光催化分解水制氢:2H2O(l) = 2H2(g)+ O2(g) ΔH2 = 571.6 kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g) = CO(g)+3H2(g) ΔH3 = 206.1 kJ·mol–1
①焦炭与水反应制氢:C(s)+ H2O(g) = CO(g)+ H2(g) ΔH1 = 131.3 kJ·mol–1
②太阳光催化分解水制氢:2H2O(l) = 2H2(g)+ O2(g) ΔH2 = 571.6 kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g) = CO(g)+3H2(g) ΔH3 = 206.1 kJ·mol–1
| A.反应①为放热反应 |
| B.反应②中电能转化为化学能 |
| C.若反应③使用催化剂,ΔH3不变 |
| D.反应2H2(g) + O2(g) = 2H2O(g)的ΔH = -571.6 kJ·mol–1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


