解答题-结构与性质 适中0.65 引用6 组卷608
由IIA元素与VA元素所形成的化合物种类繁多,它们是探测器、激光器、微波器的重要材料。回答下列问题:
(1)基态Ga原子核外电子排布式为[Ar]______ 。
(2)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为________ ,电子重排后的氧原子能量有所升高,原因是不符合_____ (填“泡利原理”或“洪特规则”)。
(3)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原因是______ 。
(4)比较大小:键角PH3________ (填“>”或“<”,下同)NH3;熔、沸点:PH3_______ NH3。
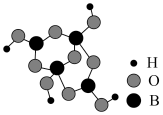
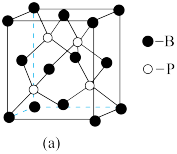
(5)如图为四硼酸根离子球棍模型,该离子符号为_______ ,其中硼原子轨道的杂化类型有______ 。
(6)叠氮酸铵(NH4N3)是一种具有爆炸性的无色晶体。叠氮酸根( )的空间结构为
)的空间结构为______ ;叠氮酸铵的晶胞如图所示,其晶胞参数为a nm和0.5a nm,阿伏加德罗常数的值为NA,NH4N3的密度为____ g·cm-3。

(1)基态Ga原子核外电子排布式为[Ar]
(2)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为
(3)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原因是
| 化学键 | B-H | B-O | B-B |
| 键能(kJ∙mol-1) | 389 | 561 | 293 |
(5)如图为四硼酸根离子球棍模型,该离子符号为

(6)叠氮酸铵(NH4N3)是一种具有爆炸性的无色晶体。叠氮酸根(

20-21高三·河南·阶段练习
类题推荐
由第ⅢA和第ⅤA元素所形成的化合物种类繁多,它们是探测器、激光器、微波器的重要材料,请根据材料回答以下问题:
(1)基态As原子的电子排布式为[Ar]___________ 。N、P、As的第一电离能从大到小的顺序是:___________ 。
(2)除了已知的氮气,科学家还先后研究出了 、
、 、
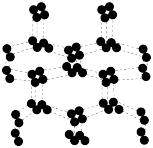
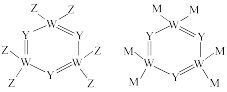
、 、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则
、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则 的沸点
的沸点___________ (填“>”、“<”或“=”)高聚氮的沸点,原因是___________ 。
(3)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为___________ ,电子重排后的氧原子能量有所升高,原因是不符合___________ (填“泡利原理”或“洪特规则”)。
(4)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的化合物,根据下表数据分析原因是___________ 。
(5) 晶体的晶胞参数为
晶体的晶胞参数为 ,
, ,α=β=90°,
,α=β=90°, =120°,结构如下图:
=120°,结构如下图:
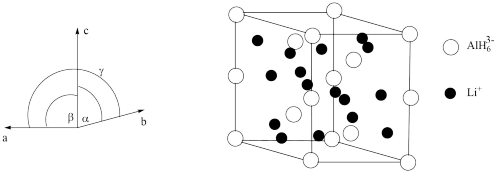
①已知 的分数坐标为(0,0,0)、(0,0,
的分数坐标为(0,0,0)、(0,0, ),(
),( ,
, ,
, ),(
),( ,
, ,
, ),(
),( ,
, ,
, )和 (
)和 ( ,
, ,
, ),晶胞中
),晶胞中 的个数为
的个数为___________ 。
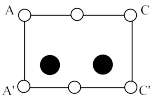
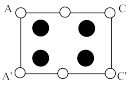
②下图是上述 晶胞的某个截面,共含有10个
晶胞的某个截面,共含有10个 ,其中6个已经画出(图中的○)请在图中用○将剩余的
,其中6个已经画出(图中的○)请在图中用○将剩余的 画出。
画出。___________

③此晶体的密度为___________ g/cm3 (列出计算式即可)。
(1)基态As原子的电子排布式为[Ar]
(2)除了已知的氮气,科学家还先后研究出了

(3)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为
(4)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的化合物,根据下表数据分析原因是
| 化学键 | |||
| 键能 (kJ/mol) | 389 | 561 | 293 |
(5)

①已知
②下图是上述

③此晶体的密度为
Ⅰ.主族元素能形成多种化合物,它们是探测器、激光器、微波器的重要材料。
(1)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为___________ ,电子重排后的氧原子能量有所升高,原因是不符合___________ (填“泡利原理”或“洪特规则”)。
(2)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原因是___________ 。
(3)NH3与BF3气体相遇发生反应生成F3B-NH3晶体
①F3B-NH3晶体中,B原子的杂化轨道类型为___________ 。
②F3B-NH3晶体中不存在的作用力有___________ 。
a.σ键 b.π键 c.离子键 d.配位键 e.范德华力
(4)已知:
解释表中物质之间沸点差异的原因___________ 。
Ⅱ.储氢合金能有效解决氢气的储存和运输,对大规模使用氢能具有重要意义。
(5)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示。M是___________ (填元素符号),判断理由是___________ 。
(6)过渡金属Q与镧(La)形成的合金也是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-1;该合金的晶胞结构和z轴方向的投影图如图所示。
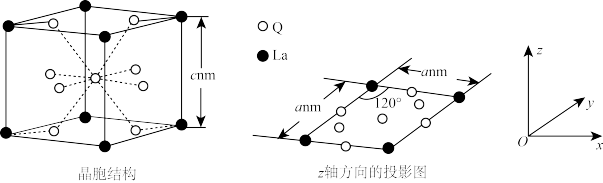
若阿伏加德罗常数的值为NA,则该合金的密度ρ=___________ g·cm-3(用含a、c、NA的代数式表示,列出计算式即可)。
(1)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为
(2)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原因是
| 化学键 | B-H | B-O | B-B |
| 键能(kJ·mol-1) | 389 | 561 | 293 |
①F3B-NH3晶体中,B原子的杂化轨道类型为
②F3B-NH3晶体中不存在的作用力有
a.σ键 b.π键 c.离子键 d.配位键 e.范德华力
(4)已知:
| 物质 | AsF3 | AsCl3 | BiF3 |
| 沸点/℃ | 62.8 | 130.2 | 900.0 |
Ⅱ.储氢合金能有效解决氢气的储存和运输,对大规模使用氢能具有重要意义。
(5)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示。M是
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |

若阿伏加德罗常数的值为NA,则该合金的密度ρ=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 B.
B.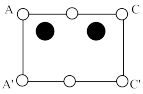 C.
C.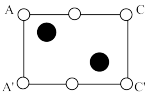 D.
D.