解答题-结构与性质 适中0.65 引用1 组卷144
许多元素及它们的化合物在科学研究和工业生产中具有许多用途。请回答下列有关问题:
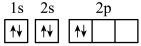
(1)某同学画出基态碳原子的轨道表示式: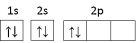 ,该表示式违背了
,该表示式违背了___ ;CH 、-CH3、CH
、-CH3、CH 都是重要的有机反应中间体。CH
都是重要的有机反应中间体。CH 的空间构型为
的空间构型为____ ;CH 中C原子成键的杂化方式为
中C原子成键的杂化方式为_____ 。
(2)34号元素硒的基态原子的价层电子排布式为_______ 。
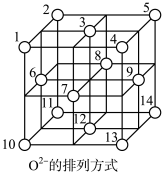
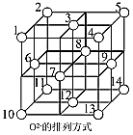
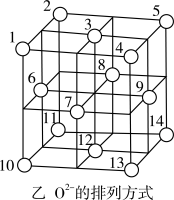
(3)Fe3O4晶体中,O2-围成正四面体空隙(1、3、6、7号氧围成)和正八面体空隙(3、6、7、8、9、12号氧围成),Fe3O4中有一半的Fe3+填充在正四面体空隙中,Fe2+和另一半Fe3+填充在正八面体空隙中,晶体中正四面体空隙数与正八面体空隙数之比为_____ ,有_____ %的正八面体空隙没有填充阳离子。
(4)白铜(铜镍合金)的立方晶胞结构如图所示,其中原子A的坐标参数为(0,1,0)。
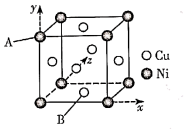
①原子B的坐标参数为____ ;
②若该晶体密度为dg·cm-3,则铜镍原子间最短距离为____ 。
(1)某同学画出基态碳原子的轨道表示式:
 ,该表示式违背了
,该表示式违背了(2)34号元素硒的基态原子的价层电子排布式为
(3)Fe3O4晶体中,O2-围成正四面体空隙(1、3、6、7号氧围成)和正八面体空隙(3、6、7、8、9、12号氧围成),Fe3O4中有一半的Fe3+填充在正四面体空隙中,Fe2+和另一半Fe3+填充在正八面体空隙中,晶体中正四面体空隙数与正八面体空隙数之比为

(4)白铜(铜镍合金)的立方晶胞结构如图所示,其中原子A的坐标参数为(0,1,0)。

①原子B的坐标参数为
②若该晶体密度为dg·cm-3,则铜镍原子间最短距离为
20-21高三·四川成都·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
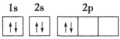 ,该电子排布图违背了
,该电子排布图违背了
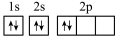 ,该电子排布图违背了
,该电子排布图违背了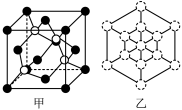
 表示P 原子的投影),用
表示P 原子的投影),用 画出B原子的投影位置
画出B原子的投影位置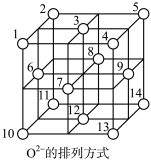
 ,该电子排布图违背了
,该电子排布图违背了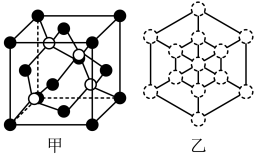
 表示P原子的投影),用
表示P原子的投影),用 画出B原子的投影位置
画出B原子的投影位置