解答题-实验探究题 适中0.65 引用5 组卷336
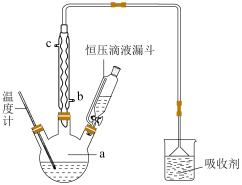
苯乙腈主要用作农药、医药、染料和香料的中间体,某学习小组在通风橱中制备苯乙腈的反应原理和主要实验装置如图:
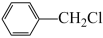 (氯化苄)+NaCN
(氯化苄)+NaCN
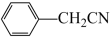 +NaCl
+NaCl
已知:苯乙腈具有刺激性,毒性作用与氢氰酸(易挥发)相似;氯化苄的密度为1.1g•mL-1,为具有强烈刺激性气味的有毒液体。制备苯乙腈时会有异腈(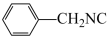 )生成,
)生成, 在酸性溶液中被水解成
在酸性溶液中被水解成 和甲酸,
和甲酸, 、甲酸均可溶于水。有关信息如表所示:
、甲酸均可溶于水。有关信息如表所示:
实验步骤如下:
①取100mL的烧杯,用10mL乙醇与11.5mL氯化苄配制混合液,将混合液小心加入a中;
②把适量二甲胺加入a中;
③向室温下的混合液中逐滴加入足量1mol·L-1NaCN溶液,边滴边搅拌,混合均匀,在80~100℃下发生反应,直至反应结束;
④将反应液减压蒸馏得到苯乙腈粗品,将粗品倒入分液漏斗中,加入等量的50%硫酸激烈摇动除去异腈后,依次用碳酸氢钠溶液和饱和食盐水洗涤,并分液;
⑤往分出的产物中加入无水CaCl2颗粒,静置片刻,然后倒入蒸馏烧瓶中,弃去CaCl2,进行蒸馏纯化,收集得到纯苯乙腈9.36g。
回答下列问题:
(1)图中仪器a的名称是___ ,倒置漏斗的作用是___ 。
(2)乙醇在反应中起溶剂的作用,能否用水代替乙醇作溶剂?___ (填“是”或“否”)。制备实验在通风橱中进行的目的是___ ,为了使反应在80~100℃下进行,常用的加热方法是___ 。
(3)球形冷凝管的出水口为__ (填“b”或“c”);为除去异腈,能否将反应液加入到浓硫酸中,并说明理由:__ 。
(4)在洗涤操作中,碳酸氢钠溶液的作用是___ ;无水CaCl2颗粒的作用是___ 。
(5)在蒸馏纯化过程中,因苯乙腈的沸点为233.5℃,应选用空气冷凝管,不选用直形冷凝管的原因是__ 。
(6)本实验所得到的苯乙腈产率是__ 。
 (氯化苄)+NaCN
(氯化苄)+NaCN +NaCl
+NaCl
已知:苯乙腈具有刺激性,毒性作用与氢氰酸(易挥发)相似;氯化苄的密度为1.1g•mL-1,为具有强烈刺激性气味的有毒液体。制备苯乙腈时会有异腈(
 )生成,
)生成, 在酸性溶液中被水解成
在酸性溶液中被水解成 和甲酸,
和甲酸, 、甲酸均可溶于水。有关信息如表所示:
、甲酸均可溶于水。有关信息如表所示:| 名称 | 相对分子质量 | 颜色、状态 | 溶解性 | 熔点/℃ | 沸点/℃ |
| 苯乙腈 | 117 | 无色油状液体 | 不溶于水,溶于醇 | -23.8 | 233.5 |
| 氯化苄 | 126.5 | 无色或微黄色的透明液体 | 微溶于水,可混溶于乙醇 | -39 | 179.4 |
| 乙醇 | 46 | 无色的液体、粘稠度低 | 与水混溶 | -114 | 78 |
| 二甲胺 | 45 | 无色气体,高浓度的带有氨味 | 易溶于水,溶于乙醇 | -92.2 | 6.9 |
①取100mL的烧杯,用10mL乙醇与11.5mL氯化苄配制混合液,将混合液小心加入a中;
②把适量二甲胺加入a中;
③向室温下的混合液中逐滴加入足量1mol·L-1NaCN溶液,边滴边搅拌,混合均匀,在80~100℃下发生反应,直至反应结束;
④将反应液减压蒸馏得到苯乙腈粗品,将粗品倒入分液漏斗中,加入等量的50%硫酸激烈摇动除去异腈后,依次用碳酸氢钠溶液和饱和食盐水洗涤,并分液;
⑤往分出的产物中加入无水CaCl2颗粒,静置片刻,然后倒入蒸馏烧瓶中,弃去CaCl2,进行蒸馏纯化,收集得到纯苯乙腈9.36g。
回答下列问题:
(1)图中仪器a的名称是
(2)乙醇在反应中起溶剂的作用,能否用水代替乙醇作溶剂?
(3)球形冷凝管的出水口为
(4)在洗涤操作中,碳酸氢钠溶液的作用是
(5)在蒸馏纯化过程中,因苯乙腈的沸点为233.5℃,应选用空气冷凝管,不选用直形冷凝管的原因是
(6)本实验所得到的苯乙腈产率是
2021·河北·模拟预测
类题推荐
实验室制备硝基苯的反应原理和实验装置: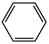 +HO-NO2
+HO-NO2
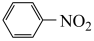 +H2O△H<0,反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。有关数据如下表:
+H2O△H<0,反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。有关数据如下表:
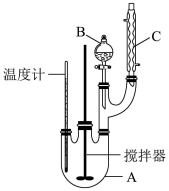
实验步骤如下:①取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混合酸,将混合酸小心加入B中;②把18mL(15.84g)苯加入A中;③向室温下的苯中逐滴加入混合酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束;④将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液、水洗涤并分液;⑤分出的产物加入无水CaCl2颗粒,静置片刻,然后倒入蒸馏烧瓶,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。回答下列问题:
(1)图中装置C的作用是____________ 。
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:____________ 。
(3)为了使反应在50~60℃下进行,常用的方法是____________ 。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是____________ 。
(4)在洗涤操作中,第二次水洗的作用是____________ 。
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用水直形冷凝管的原因是____________ 。
(6)本实验所得到的硝基苯产率是____________ 。
 +HO-NO2
+HO-NO2 +H2O△H<0,反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。有关数据如下表:
+H2O△H<0,反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。有关数据如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
实验步骤如下:①取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混合酸,将混合酸小心加入B中;②把18mL(15.84g)苯加入A中;③向室温下的苯中逐滴加入混合酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束;④将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液、水洗涤并分液;⑤分出的产物加入无水CaCl2颗粒,静置片刻,然后倒入蒸馏烧瓶,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。回答下列问题:
(1)图中装置C的作用是
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:
(3)为了使反应在50~60℃下进行,常用的方法是
(4)在洗涤操作中,第二次水洗的作用是
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用水直形冷凝管的原因是
(6)本实验所得到的硝基苯产率是
实验室制备硝基苯的实验装置如下:
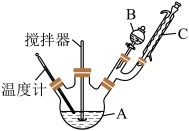
反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。有关数据如下表:
实验步骤如下:
①取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合酸,将混合酸小心加入B中;
②把18 mL (15.84 g)苯加入A中;
③在室温下,向苯中逐滴加入混合酸,边滴边搅拌,混合均匀。在50~60 ℃下发生反应,直至反应结束;
④将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液、水洗涤并分液;
⑤分出的产物加入无水CaCl2颗粒,静置片刻,然后倒入蒸馏烧瓶,弃去CaCl2,进行蒸馏纯化,收集205~210 ℃馏分,得到纯硝基苯18 g。回答下列问题:
(1)图中仪器A的名称:_________ ,装置C的作用是__________ 。
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中并说明理由:___________ 。
(3)为了使反应在50~60 ℃下进行,常用的方法是__________ ,A中发生的主要有机反应方程式是:___________ ,反应结束并冷却至室温后A中液体呈黄色,原因是__________ 。
(4)在洗涤操作中,NaOH溶液洗的目的是_____________ 。
(5)本实验所得到的硝基苯产率是_____________ 。

反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。有关数据如下表:
物质 | 熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 | 83 | 1.4 | 易溶于水 | |
浓硫酸 | 338 | 1.84 | 易溶于水 |
实验步骤如下:
①取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合酸,将混合酸小心加入B中;
②把18 mL (15.84 g)苯加入A中;
③在室温下,向苯中逐滴加入混合酸,边滴边搅拌,混合均匀。在50~60 ℃下发生反应,直至反应结束;
④将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液、水洗涤并分液;
⑤分出的产物加入无水CaCl2颗粒,静置片刻,然后倒入蒸馏烧瓶,弃去CaCl2,进行蒸馏纯化,收集205~210 ℃馏分,得到纯硝基苯18 g。回答下列问题:
(1)图中仪器A的名称:
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中并说明理由:
(3)为了使反应在50~60 ℃下进行,常用的方法是
(4)在洗涤操作中,NaOH溶液洗的目的是
(5)本实验所得到的硝基苯产率是
某科学小组制备硝基苯的实验装置如图:
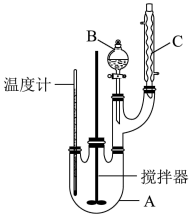
有关数据列如下表。已知存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。
实验步骤如下:
①取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制混和酸,将混合酸小心加入B中。把18mL(15.84g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
②将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)仪器A的名称是_____ ,图中装置C的作用是_____ 。
(2)制备硝基苯的化学方程式_____ 。
(3)配制混合酸时,能否将浓硝酸加入到浓硫酸中______ (“是”或“否”),说明理由:_____ 。
(4)为了使反应在50~60℃下进行,常用的方法是_____ 。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是_____ (用化学方程式说明)。
(5)本实验所得到的硝基苯产率是_____ (保留两位有效数字)。

有关数据列如下表。已知存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
实验步骤如下:
①取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制混和酸,将混合酸小心加入B中。把18mL(15.84g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
②将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)仪器A的名称是
(2)制备硝基苯的化学方程式
(3)配制混合酸时,能否将浓硝酸加入到浓硫酸中
(4)为了使反应在50~60℃下进行,常用的方法是
(5)本实验所得到的硝基苯产率是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


