解答题-工业流程题 适中0.65 引用1 组卷159
钨是熔点最高的金属,在国民经济和国防军工领域具有重要用途。工业上用白钨矿(主要成分是CaWO4)生产金属钨粉的流程如图:
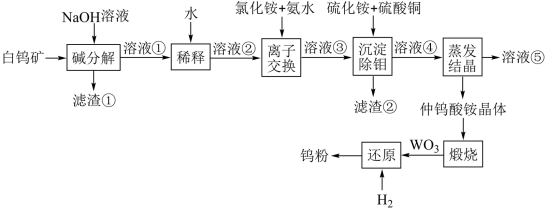
请根据上述流程回答以下问题:
(1)白钨矿与氢氧化钠反应的其中一个产物是可溶于水的钨酸钠,写出该化学反应方程式:_____ 。
(2)溶液②为钨酸钠溶液,经离子交换后得到溶液③为钨酸铵溶液,该过程中加入氨水的作用是调节溶液的pH和_____ 。
(3)溶液④为钨酸铵溶液,其经过蒸发结晶后得到仲钨酸铵[(NH4)10W12O41·5H2O]晶体,结晶过程中钨酸铵溶液没有完全蒸干,还得到溶液⑤,主要原因是_____ 。
(4)溶液⑤进入“离子交换”中循环使用,其目的为_____ (填编号)。
A.转变为钨酸铵 B.回收硫酸铵 C.提升钨的收率 D.富集钨元素
(5)请写出仲钨酸铵煅烧分解的反应方程式:_____ 。
(6)“沉淀除钼”,先加入硫化铵,把钼酸铵转化为硫代钼酸铵,再加入硫酸铜。加入硫酸铜溶液的作用是_____ 。(填编号)。
A.生成CuS沉淀,除去多余的硫化铵
B.生成硫代钼酸铜沉淀而除去
C.生成更多的钨酸铵
D.氧化钼酸铵,形成沉淀而除去
(7)用氢气或Al均可还原WO3,为得到纯度较高的产品,应选择的方法是_____ (填“氢气还原”或“Al还原”)。

请根据上述流程回答以下问题:
(1)白钨矿与氢氧化钠反应的其中一个产物是可溶于水的钨酸钠,写出该化学反应方程式:
(2)溶液②为钨酸钠溶液,经离子交换后得到溶液③为钨酸铵溶液,该过程中加入氨水的作用是调节溶液的pH和
(3)溶液④为钨酸铵溶液,其经过蒸发结晶后得到仲钨酸铵[(NH4)10W12O41·5H2O]晶体,结晶过程中钨酸铵溶液没有完全蒸干,还得到溶液⑤,主要原因是
(4)溶液⑤进入“离子交换”中循环使用,其目的为
A.转变为钨酸铵 B.回收硫酸铵 C.提升钨的收率 D.富集钨元素
(5)请写出仲钨酸铵煅烧分解的反应方程式:
(6)“沉淀除钼”,先加入硫化铵,把钼酸铵转化为硫代钼酸铵,再加入硫酸铜。加入硫酸铜溶液的作用是
A.生成CuS沉淀,除去多余的硫化铵
B.生成硫代钼酸铜沉淀而除去
C.生成更多的钨酸铵
D.氧化钼酸铵,形成沉淀而除去
(7)用氢气或Al均可还原WO3,为得到纯度较高的产品,应选择的方法是
20-21高三下·江西·阶段练习
类题推荐
锰及其化合物在现代工业和国防建设中具有十分重要的地位。金属锰的提炼方式主要有热还原法和电解法两种,热还原法得到的锰纯度在95-98%之间,电解法得到的锰(简称电解锰),其纯度可达99.7~99.9%以上。
(1)锰锌铁氧体是当前广泛使用的一种隐形涂料,其化学组成为MnxZn1-xFe2O4(铁为+3价),其中当锰锌铁氧体中n(Zn):n(Fe)=2:5时,它对雷达波的吸收能力最强。
① 锰锌铁氧体中锰元素的化合价为_______ 。
② 当雷达波吸收能力最强时,该物质的化学式为________ (改写成氧化物的形式)。
(2)写出以MnO2和Al粉为原料,利用热还原法制备Mn的化学方程式:________ 。
(3)工业上以菱锰矿(主要成分是MnCO3,含有Fe2+、Co2+、Ni2+等杂质金属离子)为原料制备电解锰的流程图如下所示。
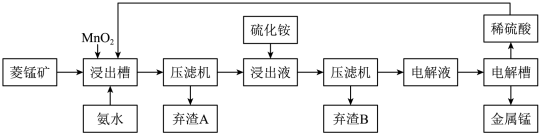
生成氢氧化物的pH如下表:
① 浸出槽中发生多个反应:如主要成分与硫酸的反应、MnO2与Fe2+间的氧化还原反应等,写出这两个反应的离子方程式:___________________ 、____________________ 。
② 加入氨水的目的是为除去杂质,根据流程图及表中数据,pH 应调控在_____ 范围内。常温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=4时溶液中c(Fe3+)=__________ 。
③ 加入硫化铵是为除去剩余的Ni2+,反应的离子方程式为____________________ 。
④ 写出电解硫酸锰溶液制取金属锰的化学方程式:________________________ 。
(1)锰锌铁氧体是当前广泛使用的一种隐形涂料,其化学组成为MnxZn1-xFe2O4(铁为+3价),其中当锰锌铁氧体中n(Zn):n(Fe)=2:5时,它对雷达波的吸收能力最强。
① 锰锌铁氧体中锰元素的化合价为
② 当雷达波吸收能力最强时,该物质的化学式为
(2)写出以MnO2和Al粉为原料,利用热还原法制备Mn的化学方程式:
(3)工业上以菱锰矿(主要成分是MnCO3,含有Fe2+、Co2+、Ni2+等杂质金属离子)为原料制备电解锰的流程图如下所示。

生成氢氧化物的pH如下表:
物质 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀时pH | 7.5 | 2.l | 7.7 | 7.6 | 8.3 |
| 完全沉淀时pH | 9.7 | 3.7 | 8.5 | 8.2 | 9.8 |
② 加入氨水的目的是为除去杂质,根据流程图及表中数据,pH 应调控在
③ 加入硫化铵是为除去剩余的Ni2+,反应的离子方程式为
④ 写出电解硫酸锰溶液制取金属锰的化学方程式:
以菱锰矿(主要成分MnCO3,还含有FeCO3、CaCO3、SiO2、Al2O3、Fe2O3、MgCO3等杂质)为原料制备二氧化锰的工艺流程如图:

已知:Ksp(MnCO3)=1.8×10-11、Ksp[Fe(OH)3]=2.8×10-39、Ksp[Al(OH)3]=1.3×10-33、Ksp(MgF2)=7.0×10-11、Ksp(CaF2)=1.0×10-10、Ksp(MnF2)=5.0×10-3。
(1)酸浸时为了提高浸出效率,除升温外,还可以采取_______ 措施。
(2)“中和除杂1”是将铁、铝元素转化为沉淀除去,物质X最好选用_______(填编号)。
(3)“除杂2”除去的主要离子是_______ (填离子符号)。
(4)“产品2”为电解过程产生的气体副产物,该气体为_______ 。
(5)工业上采用如下图的电解法获得MnO2,Mn2+将在_______ 极(填“C”或“D”)发生反应生成MnO2,其电极反应式为_______ 。电解过程中穿过离子交换膜的离子和移动方向为_______ 。 
(6)电解后的废水经过处理后,依然存在Mn2+。向含有0.020mol·L-lMn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS-浓度为1.0×10-4mol·L-1时,Mn2+开始沉淀,则a=_______ 。(已知:H2S的电离常数K1=1.0×10-7,K2=-7.0×10-15;Ksp(MnS)=1.4×10-15]

已知:Ksp(MnCO3)=1.8×10-11、Ksp[Fe(OH)3]=2.8×10-39、Ksp[Al(OH)3]=1.3×10-33、Ksp(MgF2)=7.0×10-11、Ksp(CaF2)=1.0×10-10、Ksp(MnF2)=5.0×10-3。
(1)酸浸时为了提高浸出效率,除升温外,还可以采取
(2)“中和除杂1”是将铁、铝元素转化为沉淀除去,物质X最好选用_______(填编号)。
| A.CuO | B.CuCO3 | C.Fe(OH)3 | D.MnCO3 |
(4)“产品2”为电解过程产生的气体副产物,该气体为
(5)工业上采用如下图的电解法获得MnO2,Mn2+将在

(6)电解后的废水经过处理后,依然存在Mn2+。向含有0.020mol·L-lMn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS-浓度为1.0×10-4mol·L-1时,Mn2+开始沉淀,则a=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网