单选题 适中0.65 引用2 组卷402
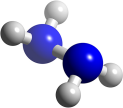
肼 是火箭常用的高能燃料,其球棍模型如图所示。肼能与双氧水发生反应:
是火箭常用的高能燃料,其球棍模型如图所示。肼能与双氧水发生反应: 。用
。用 表示阿伏加德罗常数的值,下列说法中正确的是
表示阿伏加德罗常数的值,下列说法中正确的是

| A.标准状况下, |
| B.标准状况下, |
| C.标准状况下, |
| D.若生成 |
2021·陕西咸阳·一模
类题推荐
肼(N2H4)是火箭燃料,常温下为液体,其分子的球棍模型如下图所示。肼能与双氧水发生反应:N2H4+2H2O2===N2+4H2O。下列说法正确的是

| A.11.2L N2中含电子总数为7×6.02×1023 |
| B.3.2gN2H4中含有共价键的总数为6×6.02×1022 |
| C.标准状况下,22.4LH2O2中所含原子总数为4×6.02×1023 |
| D.若生成3.6gH2O,则上述反应转移电子的数目为2×6.02×1022 |
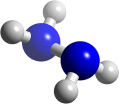
肼(N2H4)又称联氨,是火箭常用的高能燃料,常温下为液体,其球棍分子模型如图所示。肼能与双氧水发生反应 N2H4+2H2O2=N2+4H2O,用 NA表示阿伏加 德罗常数的值。下列说法正确的是

| A.N2H4属于共价化合物,分子中只含有极性共价键 |
| B.标准状况下,22.4 L N2H4中含有的原子总数为 6NA |
| C.标准状况下,3.2 g N2H4中含有共价键的总数为 0.6NA |
| D.若生成 3.6g H2O,则上述反应转移电子的数目为 0.2NA |
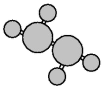
肼(N2H4)是火箭常用的高能燃料,标准状况下为液体,其球棍模型如图所示,肼与双氧水的反应为N2H4+2H2O2=N2↑+4H2O。下列说法正确的是

| A.标准状况下,11.2LN2H4中含电子总数为5NA |
| B.标准状况下,22.4LN2H4中所含原子总数为6NA |
| C.3.2gN2H4中含有共价键的总数为0.6NA |
| D.若生成3.6gH2O,则反应转移电子的数目为0.2NA |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


