解答题-原理综合题 适中0.65 引用1 组卷435
在食品行业中,N2O 可用作发泡剂和密封剂。
(1)N2O 在金粉表面发生热分解反应:2N2O(g)=2N2(g)+O2(g) ΔH
已知:2NH3(g)+3N2O(g)=4N2(g)+3H2O(l) ΔH1=-1010 kJ•mol-1
4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH2=-1531 kJ•mol-1
则 ΔH=_______ 。
(2)N2O和CO是环境污染性气体,研究表明,CO与N2O在Fe+作用下发生反应 N2O(g)+CO(g)⇌CO2(g)+N2(g)的能量变化及反应历程如图所示。
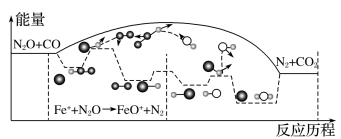
两步反应分别为:反应①Fe++N2O⇌FeO++N2,反应②_______ 。由图可知两步反应均为_______ (填“放热”或“吸热”)反应,由_______ (填“反应①”或“反应②”)决定反应达到平衡所用时间。
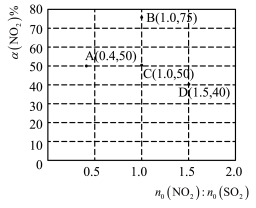
(3)在固定体积的密闭容器中,发生反应 N2O(g)+CO(g) ⇌CO2(g)+N2(g),改变原料气配比进行多组实验(各次实验的温度可能不同,也可能相同),测定 N2O 的平衡转化率。部分实验结果如图所示。
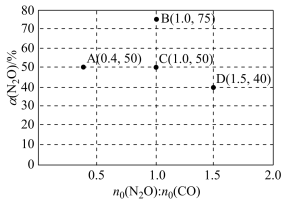
①如果要将图中 C 点的平衡状态改变为B 点的平衡状态,应采取的措施是_______ 。
②图中 C、D 两点对应的实验温度分别为 Tc和TD,通过计算判断Tc_______ (填“>”“=”或“<”)TD
(4)在某温度下,向1 L 密闭容器中充入CO与N2O,发生反应:N2O(g)+CO(g)⇌CO2(g)+N2(g),随着反应的进行,容器内 CO 的物质的量分数变化如表所示:
则该温度下反应的平衡常数 K=_______ 。
(1)N2O 在金粉表面发生热分解反应:2N2O(g)=2N2(g)+O2(g) ΔH
已知:2NH3(g)+3N2O(g)=4N2(g)+3H2O(l) ΔH1=-1010 kJ•mol-1
4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH2=-1531 kJ•mol-1
则 ΔH=
(2)N2O和CO是环境污染性气体,研究表明,CO与N2O在Fe+作用下发生反应 N2O(g)+CO(g)⇌CO2(g)+N2(g)的能量变化及反应历程如图所示。

两步反应分别为:反应①Fe++N2O⇌FeO++N2,反应②
(3)在固定体积的密闭容器中,发生反应 N2O(g)+CO(g) ⇌CO2(g)+N2(g),改变原料气配比进行多组实验(各次实验的温度可能不同,也可能相同),测定 N2O 的平衡转化率。部分实验结果如图所示。

①如果要将图中 C 点的平衡状态改变为B 点的平衡状态,应采取的措施是
②图中 C、D 两点对应的实验温度分别为 Tc和TD,通过计算判断Tc
(4)在某温度下,向1 L 密闭容器中充入CO与N2O,发生反应:N2O(g)+CO(g)⇌CO2(g)+N2(g),随着反应的进行,容器内 CO 的物质的量分数变化如表所示:
| 时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 物质的量分数 | 50.0% | 40.25% | 32.0% | 26.2% | 24.0% | 24.0% |
则该温度下反应的平衡常数 K=
2021·黑龙江哈尔滨·二模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网