解答题-原理综合题 适中0.65 引用1 组卷44
按要求填空
I.某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:___________ 与盐酸反应最剧烈,___________ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为___________ 。
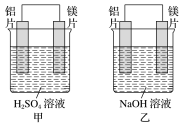
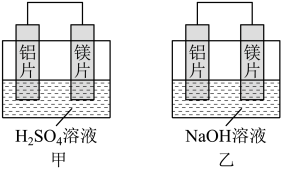
II.甲、乙两同学想利用原电池反应检验金属的活动性强弱,两人均用镁片和铝片作电极,但甲同学将两电极放入1mol/L的H2SO4溶液中,乙同学将两电极放入6mol/L的NaOH溶液中,装置如图所示。

(1)①中负极材料为___________ 。②中负极材料为___________ 。
(2)写出①中发生的正极反应式:___________ 。
I.某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
II.甲、乙两同学想利用原电池反应检验金属的活动性强弱,两人均用镁片和铝片作电极,但甲同学将两电极放入1mol/L的H2SO4溶液中,乙同学将两电极放入6mol/L的NaOH溶液中,装置如图所示。

(1)①中负极材料为
(2)写出①中发生的正极反应式:
17-18高一下·福建南平·期中
类题推荐
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/LH2SO4溶液中,乙同学将电极放入6mol/LNaOH溶液中,如图:

甲(H2SO4溶液) 乙(NaOH溶液)
(1)写出甲池中正极的电极反应式:____________________ ,负极的电极反应式:___________ 。
(2)写出乙池中负极的电极反应式:____________ ,乙池中总反应的离子方程式:__________ 。
(3)如果甲和乙同学均认为,“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出________ 活动性更强,而乙会判断出_______ 活动性更强。
(5)丙同学依据甲、乙同学的思路,设计如下实验:将铝片和铜片用导线相连.一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池。
①在这两个原电池中,负极分别为________ 。
②写出插入浓硝酸中形成原电池的总反应化学方程式__________________________________ 。

甲(H2SO4溶液) 乙(NaOH溶液)
(1)写出甲池中正极的电极反应式:
(2)写出乙池中负极的电极反应式:
(3)如果甲和乙同学均认为,“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(5)丙同学依据甲、乙同学的思路,设计如下实验:将铝片和铜片用导线相连.一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池。
①在这两个原电池中,负极分别为
| A.铝片、铜片 | B.铜片、铝片 | C.铝片、铝片 | D.铜片、铜片 |
②写出插入浓硝酸中形成原电池的总反应化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网