解答题-无机推断题 适中0.65 引用2 组卷113
化学的特征之一是从微观的层面认识物质。通过结合元素周期表与周期律,建立“位置一结构一性质”思维模型,我们可以更好地认识物质世界。
(一)X、Y、Z、M、W、Q、R是分布在周期表中三个短周期的主族元素,已知其原子半径及主要化合价如下:
(1)X在周期表中的位置是_______ ;Y、Q各自形成的简单离子中,半径较大的是_______ (填离子符号)。W和R按原子个数比1:4构成的阳离子中所含的化学键类型为_______ 。
(2)M与Z相比,非金属性较强的是_______ (填元素名称),两元素最高价氧化物的水化物中,酸性较强的是_______ (填化学式)。
(二)周期表中位于斜对角线(左上与右下)的两种元素性质十分相似,称为对角线法则。如锂与镁、铍与铝等,其单质或化合物的性质可参照对角线法则进行认识。
(3)锂在空气中燃烧主要产物的电子式是_______ 。
(4)下列关于铍的判断正确的是( )
A.氧化铍的化学式为 B.
B. 易溶于水
易溶于水
C. 是离子化合物 D.
是离子化合物 D.  具有两性
具有两性
(5) 和
和 可用试剂
可用试剂_______ 鉴别。
(一)X、Y、Z、M、W、Q、R是分布在周期表中三个短周期的主族元素,已知其原子半径及主要化合价如下:
| 元素代号 | X | Y(铝) | Z | M | W | Q | R |
| 原子半径/nm | 0.186 | 0.143 | 0.102 | 0.099 | 0.070 | 0.074 | 0.037 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
(2)M与Z相比,非金属性较强的是
(二)周期表中位于斜对角线(左上与右下)的两种元素性质十分相似,称为对角线法则。如锂与镁、铍与铝等,其单质或化合物的性质可参照对角线法则进行认识。
(3)锂在空气中燃烧主要产物的电子式是
(4)下列关于铍的判断正确的是
A.氧化铍的化学式为
C.
(5)
20-21高一·河南驻马店·阶段练习
类题推荐
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
(1)Z在元素中期表中的位置是______________________________ 。
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是__________ (填离子符号)。
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式______________________________ 。
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是____________________ 。
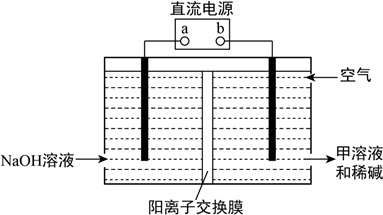
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是__________ 极,阴极的电极反应式是____________________ 。
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(1)Z在元素中期表中的位置是
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是

X、Y、Z、M、W、Q、R是分布在周期表中三个短周期的主族元素,已知其原子半径及主要化合价如下:
(1)X在周期表中的位置是____________ ;X、Y、Q各自形成的简单离子中,离子半径由大到小的顺序是___________ (填离子符号)。W和R按原子个数比 构成的粒子中所含的化学键类型为
构成的粒子中所含的化学键类型为_____________ 。
(2)X与Y相比,金属性较强的是_________ (填元素名称),两元素最高价氧化物对应的水化物中,碱性较强的是________ (填化学式)。
(3)写出X元素的最高价氧化物对应的水化物与Y的最高价氧化物反应的化学方程式:_____ 。
(4)写出实验室制取M单质的化学方程式:____________ 。
(5)下列事实能说明M元素的非金属性比Z元素的非金属性强的是______ (填字母)。
a.M单质与 溶液反应,溶液变浑浊
溶液反应,溶液变浑浊
b.在氧化还原反应中, M单质比
M单质比 Z得电子多
Z得电子多
c.M和Z两元素的简单氢化物受热分解,前者的分解温度高
| 元素代号 | X | Y(铝) | Z | M | W | Q | R |
| 原子半径/nm | 0.186 | 0.143 | 0.102 | 0.099 | 0.075 | 0.074 | 0.037 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
(2)X与Y相比,金属性较强的是
(3)写出X元素的最高价氧化物对应的水化物与Y的最高价氧化物反应的化学方程式:
(4)写出实验室制取M单质的化学方程式:
(5)下列事实能说明M元素的非金属性比Z元素的非金属性强的是
a.M单质与
b.在氧化还原反应中,
c.M和Z两元素的简单氢化物受热分解,前者的分解温度高
X、Y、Z、M、W、Q、R是7种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)上述元素中,金属性最强的在周期表中的位置是____________________ ;X、Y、Q各自形成的简单离子中,离子半径由大到小的顺序是_______ (填离子符号)。W和R按原子个数比1∶4构成的阳离子所含的化学键是________________ 。
(2)表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是_______ (填化学式),其电离方程式为_____________________________________ 。
(3)M与Z相比,非金属性较强的是_____________ (填元素名称),请从原子结构的角度说明理由________________________________________________ 。
(4)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下:
请配平,当有0.5molH2O2参加此反应,电子转移的个数为____________ 。
| 元素代号 | X | Y | Z | M | W | Q | R |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,﹣2 | +7,﹣1 | +5,﹣3 | ﹣2 | +1 |
(1)上述元素中,金属性最强的在周期表中的位置是
(2)表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是
(3)M与Z相比,非金属性较强的是
(4)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下:
请配平,当有0.5molH2O2参加此反应,电子转移的个数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


