解答题-原理综合题 适中0.65 引用1 组卷70
能源是国民经济发展的重要基础,天然气是我同目前使用的主要能源。
(1)已知:
则 的反应热
的反应热
_______  。
。
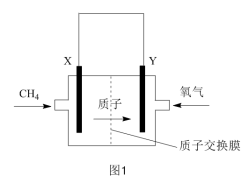
(2)燃料电池具有较高的发电效率,因而受到重视。如图1为甲烷燃料电池(电解质溶液为稀硫酸,X、Y均为Pt电极)的原理示意图,该电池的正极反应为_______ 。
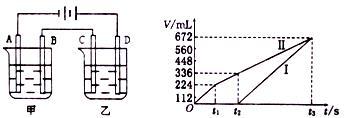
(3)利用上述燃料电池作电源,按图2所示装置进行电解,A、B、C、D均为铂电极。
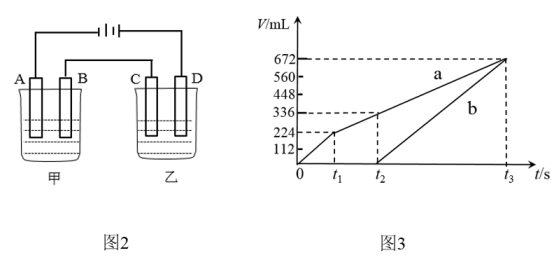
甲槽中有200mL一定浓度的NaCl与 的混合溶液,理论上两极所得气体(a和b)的体积随时间变化的关系如图3所示(气体体积已换算成标准状况下的体积)。(注意:电解前后溶液的体积变化忽略不计)
的混合溶液,理论上两极所得气体(a和b)的体积随时间变化的关系如图3所示(气体体积已换算成标准状况下的体积)。(注意:电解前后溶液的体积变化忽略不计)
①原混合溶液中NaCl的物质的量浓度为_______ mol/L。
② 时所得溶液的pH=
时所得溶液的pH=_______ 。
③工业上用电解饱和食盐水的方法制烧碱、氯气。乙槽中有足量NaCl溶液。则阳极的电极反应式为_______ ,电解的总反应式为_______ ,电解过程中,向溶液中滴加酚酞_______ 附近变红(填“阴极”或“阳极”)。
(1)已知:
| 化学键 | C-H | C=O | O=O | H-O |
| a | b | c | d |
则
(2)燃料电池具有较高的发电效率,因而受到重视。如图1为甲烷燃料电池(电解质溶液为稀硫酸,X、Y均为Pt电极)的原理示意图,该电池的正极反应为

(3)利用上述燃料电池作电源,按图2所示装置进行电解,A、B、C、D均为铂电极。

甲槽中有200mL一定浓度的NaCl与
①原混合溶液中NaCl的物质的量浓度为
②
③工业上用电解饱和食盐水的方法制烧碱、氯气。乙槽中有足量NaCl溶液。则阳极的电极反应式为
20-21高二上·黑龙江鸡西·期末
知识点:根据△H=反应物的键能之和-生成物的键能之和进行计算燃料电池原理及优点电解池电极反应式及化学方程式的书写与判断电解池有关计算 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
能量是国民经济发展的重要基础,天然气是我国目前使用的主要能源。
(1)已知
CH4(g)+2O2(g)=CO2(g)+2H2O(g)的焓变ΔH=______ kJ/mol。
(2)燃料电池具有高的发电效率,因而受到重视。下图甲为甲烷燃料电池(电解质溶液为硫酸)该电池的正极反应为_________ 。

(3)利用上述燃料电池,按下图所示装置进行电解,A、B、C、D均为铂电极,

I.甲槽中有200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如上图所示(气体体积已换算成标准状况下的体积),(电解前后溶液的体积变化关系忽略不计)
①原混合溶液中NaCl的物质的量浓度__________ mol/L。
②t2时所得溶液的pH=________ 。
Ⅱ.乙槽中为足量的AgNO3溶液。则阳极反应为__________ 。t3时电解结束,为了使溶液恢复原样,则可以在反应后的溶液中加入______ (填化学式)。
(1)已知
| 化学键 | C-H | C=O | O=O | H-O |
| E/(KJ/mol) | a | b | c | d |
CH4(g)+2O2(g)=CO2(g)+2H2O(g)的焓变ΔH=
(2)燃料电池具有高的发电效率,因而受到重视。下图甲为甲烷燃料电池(电解质溶液为硫酸)该电池的正极反应为

(3)利用上述燃料电池,按下图所示装置进行电解,A、B、C、D均为铂电极,

I.甲槽中有200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如上图所示(气体体积已换算成标准状况下的体积),(电解前后溶液的体积变化关系忽略不计)
①原混合溶液中NaCl的物质的量浓度
②t2时所得溶液的pH=
Ⅱ.乙槽中为足量的AgNO3溶液。则阳极反应为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网