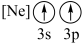解答题-结构与性质 适中0.65 引用2 组卷520
已知Mn、Fe、Co是组成合金的重要元素,P、S、Cl是农药中的重要元素。回答下列问题:
(1)Mn元素位于元素周期表的______ 区,基态锰原子的价电子排布图为_____ 。
(2)P、S、Cl三种元素的第一电离能由大到小顺序为________ 。
(3)已知NH3的沸点高于PH3,原因是________ 。
(4)农药“乐果”中的主要成分O,O-二甲基-S-(N-甲基氨基甲酰甲基)二硫代磷酸酯的分子结构为: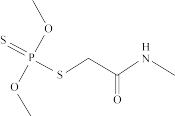 ,其中N原子的杂化类型为
,其中N原子的杂化类型为________ 。
(5)已知P4(白磷)为正四面体结构,与氧气反应生成非极性分子P4O10,其中P在空间的相对位置不变,则P4O10中σ键和π键的数目之比为_______ 。
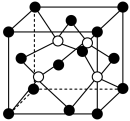
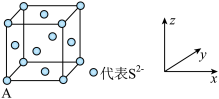
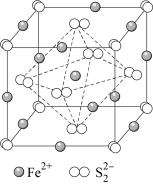
(6)已知一种立方型FeS2晶体的晶胞如图所示,则与体心Fe2+距离最近且等距离的S 的数目为
的数目为_____ 。如可用晶胞参数为单位长度建立的坐标系表示晶胞中各原子的位置,并称作原子分数坐标,则该晶胞中体心Fe2+的坐标为__________ 。
(7)已知该立方型FeS2晶体的晶胞参数为a pm,密度为d g·cm-3, 阿伏加德罗常数的值为NA,则a与d的关系是a =______ (用d、NA表示a)。
(1)Mn元素位于元素周期表的
(2)P、S、Cl三种元素的第一电离能由大到小顺序为
(3)已知NH3的沸点高于PH3,原因是
(4)农药“乐果”中的主要成分O,O-二甲基-S-(N-甲基氨基甲酰甲基)二硫代磷酸酯的分子结构为:
 ,其中N原子的杂化类型为
,其中N原子的杂化类型为(5)已知P4(白磷)为正四面体结构,与氧气反应生成非极性分子P4O10,其中P在空间的相对位置不变,则P4O10中σ键和π键的数目之比为
(6)已知一种立方型FeS2晶体的晶胞如图所示,则与体心Fe2+距离最近且等距离的S
(7)已知该立方型FeS2晶体的晶胞参数为a pm,密度为d g·cm-3, 阿伏加德罗常数的值为NA,则a与d的关系是a =

2021·贵州遵义·一模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
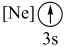 B.
B.