解答题-原理综合题 适中0.65 引用1 组卷133
CO2是温室气体,CO2的利用是解决温室效应的有效途径。试回答下列问题:
I.CO2催化制CH4
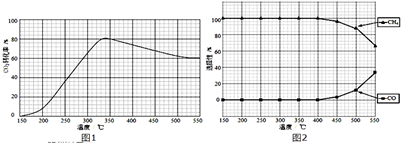
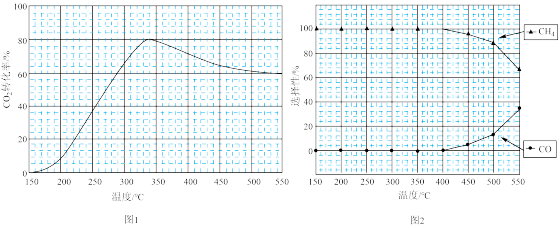
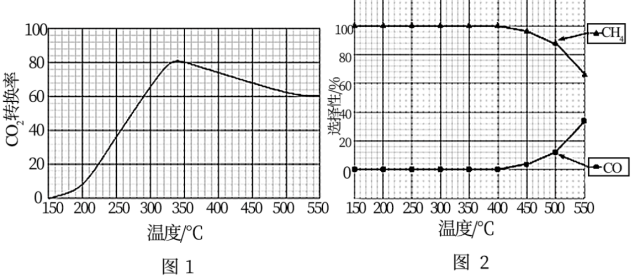
在常压,Ru/TiO2催化下,CO2和H2混合气体(体积比1:4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应I CO2(g)+4H2(g) CH4(g) + 2H2O(g) △H1
CH4(g) + 2H2O(g) △H1
反应II CO2(g) + H2(g) CO(g) + H2O(g) △H2
CO(g) + H2O(g) △H2
(1)①下列说法不正确的是___________
A.△H1小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1:3,可提高CO2平衡转化率
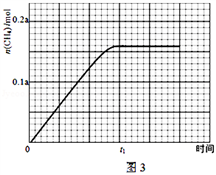
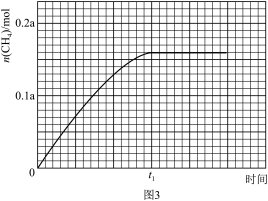
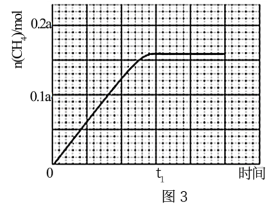
② 350℃时,反应I在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应I的平衡常数为___________ (用a、V表示)。
II.CO2电化学制CH4
(2)图3表示以KOH溶液作电解质溶液进行电解的示意图,阴极的电极反应方程式为___________ ,电解一段时间后,阳极区KOH溶液的质量分数减小,其原因是___________ 。
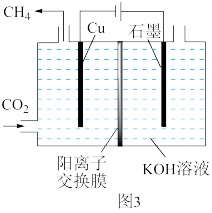
(3)甲烷可以做燃料电池,具有广阔的开发和应用前景,某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验(如图4)。
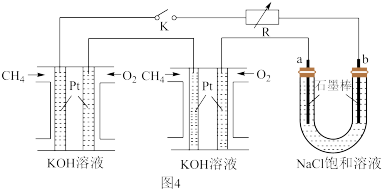
①通入甲烷气体的电极是原电池的___________ 极,其电极反应式为___________ 。
②a电极反应式为___________ 。
③如图4所示U形管中氯化钠溶液的体积为800ml。闭合K后,若每个电池甲烷用量均为22.4ml(标况),且反应完全。则理论上通过电解池的电量为___________ (单个电子的电荷量e=1.6×10-19 C,结果保留三位有效数字),若产生的气体全部逸出,电解后溶液混合均匀,温度恢复为室温,则电解后U形管中溶液的pH为___________ 。
III.CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3
(4)①Na2CO3俗称纯碱,因 水解而使其水溶液呈碱性,写出
水解而使其水溶液呈碱性,写出 第一步水解的离子方程式
第一步水解的离子方程式___________ 。已知25℃时, 第一步水解的水解常数Kh=2×10﹣4mol/L,当溶液中c(
第一步水解的水解常数Kh=2×10﹣4mol/L,当溶液中c( ):c(
):c( )=20:1时,溶液的pH=
)=20:1时,溶液的pH=___________ 。
I.CO2催化制CH4
在常压,Ru/TiO2催化下,CO2和H2混合气体(体积比1:4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应I CO2(g)+4H2(g)
反应II CO2(g) + H2(g)

(1)①下列说法不正确的是
A.△H1小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1:3,可提高CO2平衡转化率
② 350℃时,反应I在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应I的平衡常数为
II.CO2电化学制CH4
(2)图3表示以KOH溶液作电解质溶液进行电解的示意图,阴极的电极反应方程式为

(3)甲烷可以做燃料电池,具有广阔的开发和应用前景,某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验(如图4)。

①通入甲烷气体的电极是原电池的
②a电极反应式为
③如图4所示U形管中氯化钠溶液的体积为800ml。闭合K后,若每个电池甲烷用量均为22.4ml(标况),且反应完全。则理论上通过电解池的电量为
III.CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3
(4)①Na2CO3俗称纯碱,因
20-21高二下·黑龙江大庆·开学考试
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 CH4(g)+2H2O(g)△H4
CH4(g)+2H2O(g)△H4