解答题-实验探究题 适中0.65 引用4 组卷783
实验室利用SO2合成硫酰氯(SO2Cl2),并对H2SO3和HClO的酸性强弱进行探究。
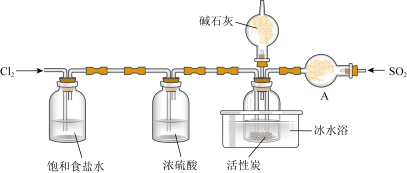
Ⅰ.已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量白雾,100℃以上分解生成SO2和Cl2.实验室合成SO2Cl2的原理:SO2(g)+Cl2(g) SO2Cl2(l) ΔH<0,实验装置如图所示(夹持仪器已省略),请回答下列问题:
SO2Cl2(l) ΔH<0,实验装置如图所示(夹持仪器已省略),请回答下列问题:
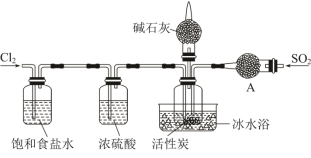
(1) 装置A中的试剂是___________ 。
(2) 活性炭的作用是___________ 。
(3) 在冰水浴中制备SO2Cl2的原因是___________ 。
(4) 为了测定SO2Cl2产品纯度(杂质不参与反应),称取a g SO2Cl2产品于锥形瓶中,加入足量蒸馏水,充分反应。用c mol·L-1 AgNO3溶液滴定反应后的溶液,滴几滴K2CrO4溶液做指示剂,当生成Ag2CrO4砖红色沉淀时,认为溶液中Cl-沉淀完全,此时消耗AgNO3溶液的体积为V mL。
①用棕色滴定管盛装AgNO3溶液,其原因是___________ 。
②该SO2Cl2产品的纯度为___________ 。
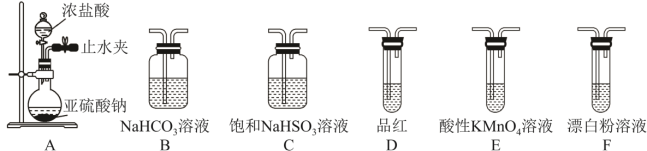
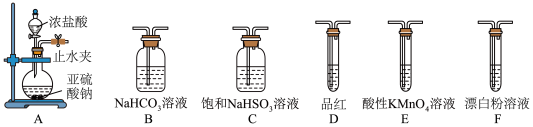
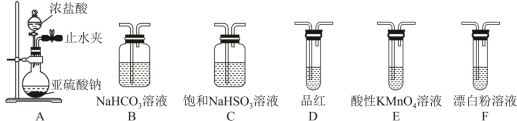
Ⅱ.(5)选用下面的装置探究酸性:H2SO3>HClO,其连接顺序为A→___________ 。能证明H2SO3的酸性强于HClO的实验现象为___________ 。
Ⅰ.已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量白雾,100℃以上分解生成SO2和Cl2.实验室合成SO2Cl2的原理:SO2(g)+Cl2(g)

(1) 装置A中的试剂是
(2) 活性炭的作用是
(3) 在冰水浴中制备SO2Cl2的原因是
(4) 为了测定SO2Cl2产品纯度(杂质不参与反应),称取a g SO2Cl2产品于锥形瓶中,加入足量蒸馏水,充分反应。用c mol·L-1 AgNO3溶液滴定反应后的溶液,滴几滴K2CrO4溶液做指示剂,当生成Ag2CrO4砖红色沉淀时,认为溶液中Cl-沉淀完全,此时消耗AgNO3溶液的体积为V mL。
①用棕色滴定管盛装AgNO3溶液,其原因是
②该SO2Cl2产品的纯度为
Ⅱ.(5)选用下面的装置探究酸性:H2SO3>HClO,其连接顺序为A→

2021·湖南永州·二模
类题推荐
实验室利用SO2合成硫酰氯(SO2Cl2),已知SO2Cl2的熔点为54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量白雾,100℃以上分解生成SO2和Cl2.实验室合成SO2Cl2的原理:
 ,实验装置如图所示(夹持仪器已省略)。请回答下列问题:
,实验装置如图所示(夹持仪器已省略)。请回答下列问题:___________ 。
(2)合成产品的装置必须干燥,否则SO2和Cl2将在水中反应,离子方程式为___________ 。
(3)将反应装置放在冰水浴中制备SO2Cl2的原因是___________ 。
(4)为了测定SO2Cl2产品纯度(杂质不参与反应),称取wgSO2Cl2产品放入锥形瓶中,加入足量蒸馏水,充分反应。用amol·L-1AgNOa3溶液滴定反应后的溶液,滴几滴K2CrO4溶液为指示剂,滴定结束时消耗AgNO3溶液的体积为VmL。
①当___________ 时,认为溶液中Cl-沉淀完全。
②该SO2Cl2产品的纯度为___________ 。
(5)下列关于该实验说法不正确的是___________。
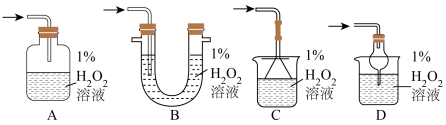
(6)停止实验后,可将SO2发生装置连接H2O2吸收装置制备稀硫酸,下列吸收装置合适的是___________ (填字母)。
(2)合成产品的装置必须干燥,否则SO2和Cl2将在水中反应,离子方程式为
(3)将反应装置放在冰水浴中制备SO2Cl2的原因是
(4)为了测定SO2Cl2产品纯度(杂质不参与反应),称取wgSO2Cl2产品放入锥形瓶中,加入足量蒸馏水,充分反应。用amol·L-1AgNOa3溶液滴定反应后的溶液,滴几滴K2CrO4溶液为指示剂,滴定结束时消耗AgNO3溶液的体积为VmL。
①当
②该SO2Cl2产品的纯度为
(5)下列关于该实验说法不正确的是___________。
| A.活性炭的作用是做吸附剂或催化剂 |
| B.装碱石灰的干燥管可以处理尾气,并防止水蒸气进入反应装置 |
| C.图中饱和食盐水也可以换成饱和NaHCO3溶液 |
| D.用AgNO3溶液滴定时,需要用棕色滴定管盛装AgNO3溶液 |
(6)停止实验后,可将SO2发生装置连接H2O2吸收装置制备稀硫酸,下列吸收装置合适的是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网