解答题-工业流程题 困难0.15 引用1 组卷1073
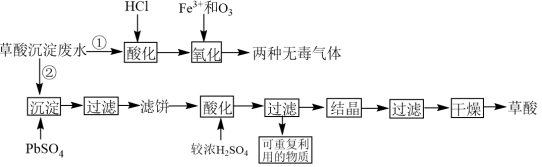
稀土工业生产中,草酸(H2C2O4)是稀土元素沉淀剂。工业生产中会产生稀土草酸沉淀废水,其主要成分为盐酸和草酸的混合溶液及微量的草酸稀土杂质等。此废水腐蚀性较强,直接排放会造成环境污染。工业上处理废水的方法包括“①氧化法”和“②沉淀法”。相关工业流程如图所示:
25℃时,各物质的溶度积常数如下表:
回答下列问题:
(1)“①氧化法”中Fe3+是反应的催化剂,反应产生了两种无毒气体。则草酸和臭氧反应的化学方程式为_______ 。
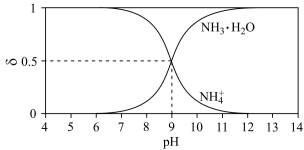
(2)“氧化”步骤中,当废水pH=1.0时,单位时间内的草酸去除率接近55%;当废水的pH上升至5.5时,单位时间内的草酸去除率只有5%,其原因是_______ 。为了使加入的17.5mg·L-1的Fe3+催化效果达到最佳,废水酸化时应将pH调整至小于_______ (已知lg2=0.3,1g5=0.7)。
(3)“②沉淀法”:将1.5mol PbSO4沉淀剂加到1L含有0.1mol·L-1草酸的模拟废水中。沉淀时发生的离子反应为PbSO4(s)+H2C2O4(aq)=PbC2O4(s)+2H+(aq)+ (aq)。请计算此反应的平衡常数K=
(aq)。请计算此反应的平衡常数K=_______ 。
(4)滤饼“酸化”“过滤”后可重复利用的物质为_______ (填化学式)。
(5)比较“①氧化法”和“②沉淀法”,从原料利用率角度分析,方法_______ (填“①”或“②”)更好,原因是_______ 。

25℃时,各物质的溶度积常数如下表:
| Ksp[Fe(OH)3] | Ksp(PbSO4) | Ksp(PbC2O4) | Ka1(H2C2O4)] | Ka2(H2C2O4) |
| 2.5×10-39 | 2.0×10-8 | 5.0×10-10 | 6.0×10-2 | 6.25×10-5 |
(1)“①氧化法”中Fe3+是反应的催化剂,反应产生了两种无毒气体。则草酸和臭氧反应的化学方程式为
(2)“氧化”步骤中,当废水pH=1.0时,单位时间内的草酸去除率接近55%;当废水的pH上升至5.5时,单位时间内的草酸去除率只有5%,其原因是
(3)“②沉淀法”:将1.5mol PbSO4沉淀剂加到1L含有0.1mol·L-1草酸的模拟废水中。沉淀时发生的离子反应为PbSO4(s)+H2C2O4(aq)=PbC2O4(s)+2H+(aq)+
(4)滤饼“酸化”“过滤”后可重复利用的物质为
(5)比较“①氧化法”和“②沉淀法”,从原料利用率角度分析,方法
21-22高三上·湖北武汉·阶段练习
类题推荐
工业上以钛铁矿(主要成分是FeTiO3,含少量SiO2、MnO2、Fe2O3、Sc2O3等)为原料制备TiO2和Sc2O3的工艺流程如下图所示。
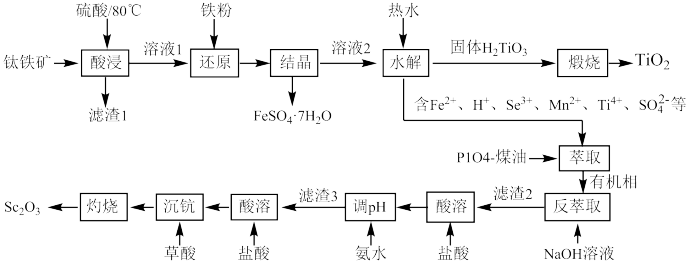
已知:Ⅰ.25℃时,一些金属氢氧化物的Ksp如表所示。
Ⅱ.25℃时,草酸的电离平衡常数为Ka1=6 ×10-2 ,Ka2=5×10-5。回答下列问题:
(1)已知溶液1中,钛以TiO2+的形式存在则FeTiO3与硫酸发生主要反应的化学方程式是_______ 。
(2)获得FeSO4·7H2O晶体的操作是_______ 、过滤( 洗涤)。
(3)若流程省去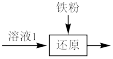 步骤,则制备的产品TiO2中含有的杂质是
步骤,则制备的产品TiO2中含有的杂质是_______ (填化学式)。
(4)“有机相”需用洗涤液(93%的硫酸、27.5%的双氧水和水按一定比例混合而成)洗涤,其作用除了除去其中剩余的钛离子外,还可使Fe2+转化为Fe3+,该转化的离子方程式是_______ 。
(5)用氨水调节溶液的pH分两步进行若溶液中c(Fe3+)=c(Se3+)=c(Mn2+)=0.1 mol·L-1,离子浓度为1×10-6mol·L-1时认为完全沉淀,则先加入氨水调节pH的范围是_______ (保留一位小数,已知lg2=0.3);过滤,继续加入氨水调节pH过滤得到的滤渣3是_______ (填化学式)。
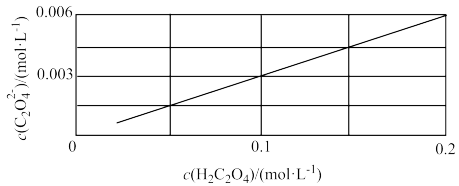
(6)25℃时用草酸“沉钪”得到Sc2(C2O4)3沉淀,溶液中c(H2C2O4)与c( )的关系如图,此时溶液的pH=
)的关系如图,此时溶液的pH=_______ 。

已知:Ⅰ.25℃时,一些金属氢氧化物的Ksp如表所示。
| 金属氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Sc(OH)3 |
| Ksp | 1.0×10-39 | 8.0×10-16 | 1.1×10-13 | 2.0×10-31 |
(1)已知溶液1中,钛以TiO2+的形式存在则FeTiO3与硫酸发生主要反应的化学方程式是
(2)获得FeSO4·7H2O晶体的操作是
(3)若流程省去
 步骤,则制备的产品TiO2中含有的杂质是
步骤,则制备的产品TiO2中含有的杂质是(4)“有机相”需用洗涤液(93%的硫酸、27.5%的双氧水和水按一定比例混合而成)洗涤,其作用除了除去其中剩余的钛离子外,还可使Fe2+转化为Fe3+,该转化的离子方程式是
(5)用氨水调节溶液的pH分两步进行若溶液中c(Fe3+)=c(Se3+)=c(Mn2+)=0.1 mol·L-1,离子浓度为1×10-6mol·L-1时认为完全沉淀,则先加入氨水调节pH的范围是
(6)25℃时用草酸“沉钪”得到Sc2(C2O4)3沉淀,溶液中c(H2C2O4)与c(

稀土在电子、激光、核工业、超导等诸多高科技领域有广泛的应用。钪(Sc)是一种稀土金属,利用钛尾矿回收金属钪和草酸的工艺流程如图1所示。回答下列问题:

已知:①xNH4Cl·yScF3·zH2O是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
③25℃时,部分物质的相关信息如表所示:
(1)“焙烧”过程生成Sc2O3的化学方程式为___________ 。
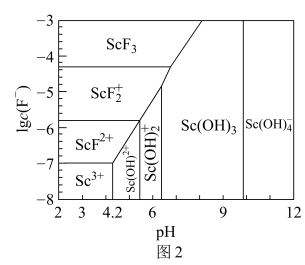
(2)含钪元素的微粒与lgc(F-)、pH的关系如下图所示,用氨水调节溶液的pH值,控制pH的范围是3.5<pH<___________ 。
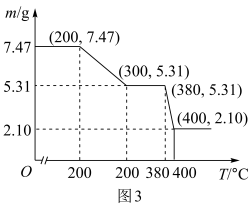
(3)“脱水除铵”过程中固体质量与温度的关系如下图所示,其中在380-400℃过程中会有白烟冒出,保温至无烟气产生,即得到 ScF3,由图3中数据可得x:z=___________ 。
(4)传统制备ScF3的方法是先得到ScF3·6H2O沉淀,再高温脱水得ScF3,但通常含有ScOF杂质,原因是___________ 。(用化学方程式表示)。流程中“沉钪”后“脱水除铵”可制得纯度很高的ScF3,其原因是___________ 。
(5)将1.8mol PbSO4加到1L含有0.12mol/L H2C2O4的废水中。发生的离子反应为PbSO4(s)+H2C2O4(aq) PbC2O4(s)+2H+(aq)+ SO
PbC2O4(s)+2H+(aq)+ SO (aq),该反应的平衡常数K=
(aq),该反应的平衡常数K=___________ 。滤饼经浓硫酸处理后的“沉淀”是___________ (化学式)。

已知:①xNH4Cl·yScF3·zH2O是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
③25℃时,部分物质的相关信息如表所示:
| Ksp(PbSO4) | Ksp(PbC2O4) | Ka1(H2C2O4) | Ka2(H2C2O4) |
| 2.0×10-8 | 5.0×10-10 | 6.0×10-2 | 6.25×10-5 |
(2)含钪元素的微粒与lgc(F-)、pH的关系如下图所示,用氨水调节溶液的pH值,控制pH的范围是3.5<pH<

(3)“脱水除铵”过程中固体质量与温度的关系如下图所示,其中在380-400℃过程中会有白烟冒出,保温至无烟气产生,即得到 ScF3,由图3中数据可得x:z=

(4)传统制备ScF3的方法是先得到ScF3·6H2O沉淀,再高温脱水得ScF3,但通常含有ScOF杂质,原因是
(5)将1.8mol PbSO4加到1L含有0.12mol/L H2C2O4的废水中。发生的离子反应为PbSO4(s)+H2C2O4(aq)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网