解答题-实验探究题 较易0.85 引用1 组卷156
浩瀚的海洋约占地球表面积的71%,它是一个巨大的宝藏。海水中水储量约为1.3×1018吨,约占地球上总水量的97%。
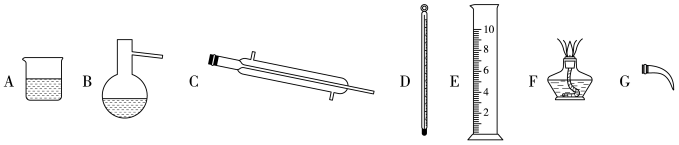
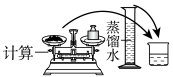
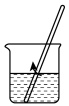
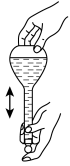
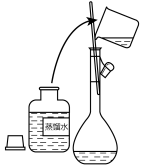
(1)海水淡化主要有蒸馏法。实验室进行水蒸馏的装置有_______ (选填必要序号)。
(2)某苦卤水中主要含有Mg2+、 、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量_______ 试剂,过滤,_______ 析晶。所得晶体中含有少量KCl杂质,简述实验检验其中Cl-的实验操作与现象_______ 。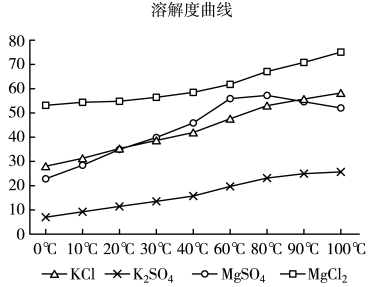
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如下:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为_______ 。
(4)配制100mL 0.2mol/LKI溶液的操作如下,请正确排序_______ (填数字序号)。
(5)溶解了CO2的水可以溶解自然界中的碳酸钙,产生含 的天然水。写出相应的离子反应方程式
的天然水。写出相应的离子反应方程式_______ 。
(6)海水中含有大量矿物质,你认为海水中会富含石油吗?_______ (填“会”或“不会”)。
(1)海水淡化主要有蒸馏法。实验室进行水蒸馏的装置有

(2)某苦卤水中主要含有Mg2+、

(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如下:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为
(4)配制100mL 0.2mol/LKI溶液的操作如下,请正确排序
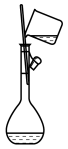 | 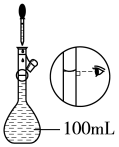 |  |  |  |  |
① | ② | ③ | ④ | ⑤ | ⑥ |
(6)海水中含有大量矿物质,你认为海水中会富含石油吗?
20-21高一上·四川成都·期中
类题推荐
浩瀚的海洋约占地球表面积的71%,它是一个巨大的宝藏,海水中水储量约为1.3×1018吨,约占地球上总水量的97%。请回答下列相关问题:
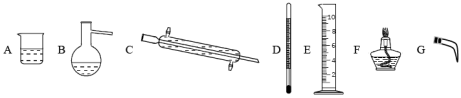
(1)海水淡化主要用蒸馏法。实验室蒸馏操作用到的主要仪器有___ (选填必要序号)。
(2)海水中主要含有Mg2+、SO 、K+、Cl-等离子,简述实验检验其中SO
、K+、Cl-等离子,简述实验检验其中SO 的实验操作与现象
的实验操作与现象___ ;简述实验检验其中Cl-的实验操作与现象___ 。
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如图:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为___ 。小铭想要配制100mL0.2mol/L的KI溶液,需称量KI的质量为___ g,实验操作示意图如图,请你将其正确排序___ (填数字序号)。
(4)海水中含有大量矿物质,你认为海水中会富含石油吗?__ (填“会”或“不会”)。
(1)海水淡化主要用蒸馏法。实验室蒸馏操作用到的主要仪器有

(2)海水中主要含有Mg2+、SO
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如图:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为
 | 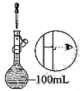 | 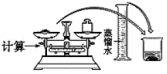 |  | 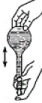 |  |
| ① | ② | ③ | ④ | ⑤ | ⑥ |
(4)海水中含有大量矿物质,你认为海水中会富含石油吗?
全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:
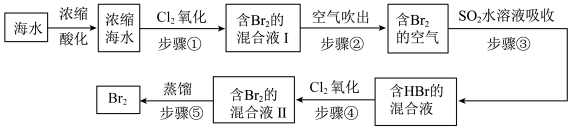
(1)步骤①中获得Br2的离子方程式为____ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是____ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收1molBr2共有___ 个电子转移(用NA的代数式表示)。
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤溶解和____ 。
(5)“试剂a”通常应具有一定的____ 性。利用H2O2完成“溶液A”向“溶液B”的转变。写出该反应的化学方程式:________________ 。
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___ 。(选填编号)
(7)“操作II”宜选用的装置是 。(选填编号)
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:____ 。
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液50.0mL,恰好反应完全。则所测盐中碘的含量是____ mg•g-1(保留四位小数)。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收1molBr2共有
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤溶解和
(5)“试剂a”通常应具有一定的
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.溴水 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水互溶与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
(7)“操作II”宜选用的装置是 。(选填编号)
A.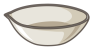 | B. | C.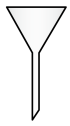 | D.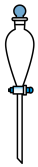 |
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液50.0mL,恰好反应完全。则所测盐中碘的含量是
我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:
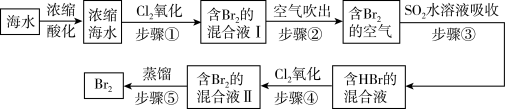
(1)步骤①中获得Br2的离子方程式为____ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是____ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2共有___ 个电子转移(用a和NA的代数式表示)。
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤:____ 、____ 。
(5)“试剂a”通常应具有一定的____ 性。
利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:____ 。
______KI+______H2O=______KOH+______I2
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___ 。(选填编号)
(7)“操作II”宜选用的装置是____ 。(选填编号)
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:____ 。
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液30.0mL,恰好反应完全。
则所测盐中碘的含量是____ mg•g-1(保留四位小数)。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2共有
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤:
(5)“试剂a”通常应具有一定的
利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:
______KI+______H2O=______KOH+______I2
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水不互溶不与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
(7)“操作II”宜选用的装置是
A. | B.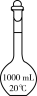 | C.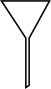 | D. |
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液30.0mL,恰好反应完全。
则所测盐中碘的含量是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


