单选题 较易0.85 引用1 组卷62
已知反应N2(g)+3H2(g)⇌2NH3(g)ΔH=﹣92.2kJ·mol﹣1。当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示。下列说法正确的是
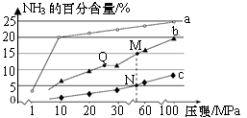

| A.若反应器中充入1molN2和3molH2,则反应达平衡时将释放92.2kJ热量 |
| B.从Q到M,平衡向左移动 |
| C.M、N、Q达到平衡所需时间关系为tQ>tM>tN |
| D.图中M、N、Q点平衡常数K的大小关系为K(N)>K(M)=K(Q) |
20-21高二上·湖北咸宁·期末
类题推荐
已知 、
、 下
下
 。在反应器中按
。在反应器中按 投料后,在不同温度下,反应达到平衡时,得到混合物中
投料后,在不同温度下,反应达到平衡时,得到混合物中 的质量分数随压强的变化曲线a、b、c如图所示。下列说法正确的是
的质量分数随压强的变化曲线a、b、c如图所示。下列说法正确的是
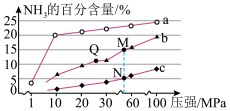

| A.图中M、N、Q点平衡常数K的大小关系为 |
| B.从Q到M,平衡向左移动 |
| C.M、N、Q达到平衡所需时间关系为 |
| D.该条件下,向反应器中充入 |
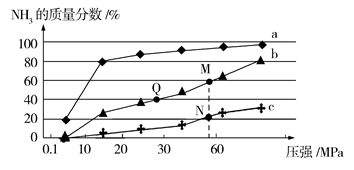
已知反应N2(g)+3H2(g) 2NH3(g) ΔH<0。按n(N2)∶n(H2) = 1∶3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
2NH3(g) ΔH<0。按n(N2)∶n(H2) = 1∶3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
 2NH3(g) ΔH<0。按n(N2)∶n(H2) = 1∶3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
2NH3(g) ΔH<0。按n(N2)∶n(H2) = 1∶3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
| A.曲线a、b、c对应的温度是由低到高 |
| B.若Q点时c(NH3) =0.4 mol·L−1,则此时反应的化学平衡常数K=50 |
| C.N点的反应速率<M点的反应速率 |
| D.M点对应H2的转化率是60% |
已知
 ,如图是恒容容器中按n(N2):n(H2)=1:3,投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中
,如图是恒容容器中按n(N2):n(H2)=1:3,投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中 的物质的量分数随压强的变化曲线。下列叙述正确的是
的物质的量分数随压强的变化曲线。下列叙述正确的是
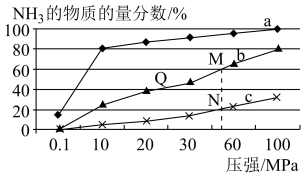

| A.曲线a对应的温度为600℃ |
| B.M点对应的H2转化率是75% |
| C.及时分离出NH3可以提高正反应速率 |
| D.图中M、N、Q点平衡常数K的大小关系是 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


