单选题 适中0.65 引用1 组卷178
根据反应情况不同,反应热可分为多种,例如燃烧热、中和热、溶解热等,下列关于燃烧热的说法不正确的是
| A.已知:S(s)+O2 (g)=SO2 (g) ΔH1=—Q1 kJ•mol-1,S(g)+O2 (g)=SO2 (g) ΔH2=—Q2 kJ•mol-1,则Q1<Q2 |
| B.已知反应C(s)+CO2 (g)= 2CO(g)的ΔH>0,则该反应在高温下能自发进行 |
| C.500℃、30MPa下,将0.5mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3,放出的热量为19.3 kJ,其热化学方程式为N2 (g)+3H2 (g) |
| D.已知中和热为—57.3 kJ•mol-1,若将含0.5 mol H2 SO4的稀溶液与含0.5 mol Ba(OH)2的稀溶液混合,放出的热量等于57.3 kJ |
20-21高二上·湖北鄂州·期末
类题推荐
下列说法正确的是
| A.甲烷燃烧的数值为890.3KJ/mol,则甲烷燃烧的化学方程式可表示为: CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ·mol-1 |
| B.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的中和热为57.4kJ/mol |
C.在500℃、20MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+2H2(g) 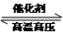 2NH3(g) △H=-38.6kJ·mol-1 2NH3(g) △H=-38.6kJ·mol-1 |
| D.已知:2C(s)+2O2(g) =2CO2(g) ΔH1,2C(s)+O2(g) =2CO(g) ΔH2,则ΔH1<ΔH2 |
下列关于热化学反应的描述中正确的是
| A.已知稀溶液中,H+(aq)+OH﹣(aq)=H2O(l) ΔH=-57.3 kJ•mol﹣1,则稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
| B.已知CO(g)的燃烧热ΔH是-283.0 kJ•mol﹣1,则2CO2(g)=2CO(g)+O2(g)反应的△H为+566 kJ•mol﹣1 |
| C.已知:①2C(s)+O2(g)=2CO(g) △H1 ②2C(s)+2O2(g)=2CO2(g)△H2,则ΔH1<ΔH2 |
| D.500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放出19.3 kJ热量,其热化学方程式为:N2(g)+3H2(g) |
下列说法正确的是
| A.已知:2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g) =2CO(g),△H2,则△H1 <ΔH2 |
| B.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ 的热量,则稀醋酸和稀NaOH溶液反应的中和热为:57.4kJ/mol |
C.在500℃,20MPa下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)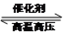 2NH3(g),△H=-38.6 kJ·mol-1 2NH3(g),△H=-38.6 kJ·mol-1 |
| D.甲烷燃烧热的数值为890.3KJ/mol,则甲烷燃烧的化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ·mol-1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


