填空题 较易0.85 引用1 组卷113
氨(NH3)、肼(N2H4)是两种氮的氢化物。
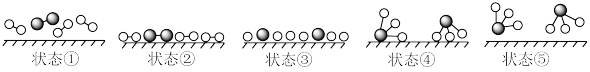
(1)合成氨的反应是一个放热反应。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如图:

状态②、③、④中,能量最高的状态是___ 。
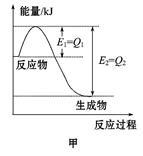
(2)已知途径Ⅰ两步转化反应的反应热分别为ΔH1、ΔH2,途径Ⅱ所示反应的反应热为ΔH,能否由途径Ⅰ的反应热推出途径Ⅱ的ΔH?___ ,(若能,请说明理由),(若不能,请说明还需补充的数据)___ 。
途径Ⅰ.N2 NH3(ΔH1)
NH3(ΔH1) NO、H2O(l)(ΔH2)
NO、H2O(l)(ΔH2)
途径Ⅱ.N2 NO(ΔH)
NO(ΔH)
(3)发射卫星时用肼(N2H4)作燃料、二氧化氮(NO2)作氧化剂。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1= +67kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2= -500kJ·mol-1
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:___ 。
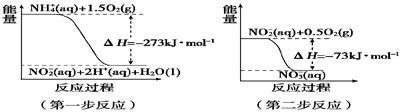
(4)在微生物的作用下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
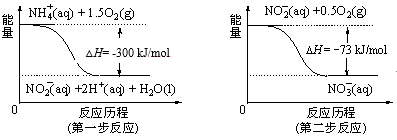
①第一步反应是___ (填“放热”或“吸热”)反应。
②1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___ 。
(1)合成氨的反应是一个放热反应。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如图:

状态②、③、④中,能量最高的状态是
(2)已知途径Ⅰ两步转化反应的反应热分别为ΔH1、ΔH2,途径Ⅱ所示反应的反应热为ΔH,能否由途径Ⅰ的反应热推出途径Ⅱ的ΔH?
途径Ⅰ.N2
途径Ⅱ.N2
(3)发射卫星时用肼(N2H4)作燃料、二氧化氮(NO2)作氧化剂。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1= +67kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2= -500kJ·mol-1
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
(4)在微生物的作用下,NH

①第一步反应是
②1molNH
20-21高二上·湖北咸宁·阶段练习
类题推荐
(1)肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,生成N2和H2O(g)。
已知:N2(g)+2O2(g)=N2O4(g) △H=+8.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.7kJ/mol ②
请写出肼跟N2O4反应的热化学反应方程式:___________________________ 。
(2)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
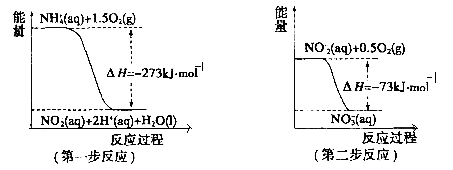
①第一步反应是__________ (填“放热”或“吸热”),判断依据是_____________ 。
②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是_________________________ 。
(3)右表是部分化学键的键能数据:
已知N2(g) +3H2(g) 2NH3(g) 试计算该反应的焓变,ΔH=
2NH3(g) 试计算该反应的焓变,ΔH= ______ (用含有a、b、c的代数式表示)。
已知:N2(g)+2O2(g)=N2O4(g) △H=+8.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.7kJ/mol ②
请写出肼跟N2O4反应的热化学反应方程式:
(2)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:

①第一步反应是
②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是
(3)右表是部分化学键的键能数据:
| 化学键 | N≡N | H-H | N-H |
| 键能/kJ ▪ mol | a | b | C |
已知N2(g) +3H2(g)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网