单选题 较难0.4 引用2 组卷368
常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
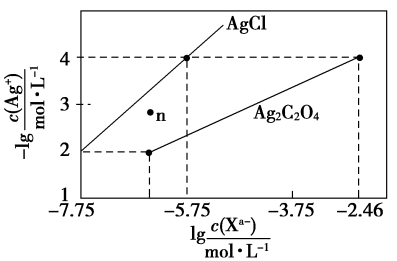

| A.Ksp(Ag2C2O4)的数量级等于10-10 |
| B.n点表示AgCl的不饱和溶液 |
| C.向c(Cl-)=c( |
| D.Ag2C2O4+2Cl-=2AgCl+ |
20-21高二上·贵州铜仁·期末
类题推荐
一定温度下,AgCl和Ag2C2O4两种难溶化合物的溶解平衡曲线如图所示,下列说法中错误的是
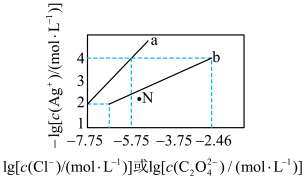
| A.a代表AgCl溶解平衡图像 |
| B.N点为Ag2C2O4的过饱和溶液 |
| C.该温度下, |
| D.向NaCl、Na2C2O4均为0.1 mol/L的混合溶液中滴加AgNO3溶液,Cl-先沉淀 |
常温下,向25 mL0.12 mol/L AgNO3溶液中逐滴加入浓度为2%的氨水,先出现沉淀,继续滴加沉淀溶解。该过程中加入氨水的体积V与溶液中lg 的关系如图所示。已知e点时溶液迅速由浑浊变得澄清,且此时溶液中c(Ag+)与c(NH3)均约为2×10-3 mol/L。下列叙述不正确的是( )
的关系如图所示。已知e点时溶液迅速由浑浊变得澄清,且此时溶液中c(Ag+)与c(NH3)均约为2×10-3 mol/L。下列叙述不正确的是( )
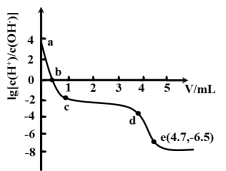

| A.a点溶液呈酸性的原因是AgNO3水解 |
| B.b点溶液中:c(Ag+)+c[Ag(NH3)2+]<c(NO3-) |
C.由e点可知,反应Ag++2NH3 [Ag(NH3)2]+平衡常数的数量级为105 [Ag(NH3)2]+平衡常数的数量级为105 |
| D.c~d段加入的氨水主要用于沉淀的生成和溶解 |
测定溶液中Cl-的浓度时,常用标准AgNO3溶液滴定,K2CrO4作指示剂。根据如下关于AgCl、Ag2CrO4的溶度积图,判断下列说法正确的是


| A.P点时,二者的溶度积常数相同 |
| B.M点时,对AgCl溶液而言为饱和状态,对Ag2CrO4溶液而言为过饱和状态 |
| C.向c(Cl-)=c( |
| D.向c(Cl-)=c( |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


