单选题 适中0.65 引用2 组卷132
下列热化学方程式中,正确的是
| A.甲烷燃烧热为890.3 kJ•mol-1,热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=+890.3 kJ•mol-1 |
| B.稀硫酸和稀氢氧化钠溶液混合,其热化学方程式为:H++OH-=H2O △H=-57.3 kJ•mol-1 |
| C.H2燃烧热为285.8kJ•mol-1,燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(1) △H=-571.6 kJ•mol-1 |
| D.500℃、30 MPa下,将1 mol N2和3 mol H2置于密闭的容器中充分反应生成NH3(g),放热38.6 kJ,其热化学方程式为:N2(g)+3H2(g) |
20-21高二上·甘肃武威·期末
类题推荐
下列热化学方程式,正确 的是( )
| A.甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
| D.500 ℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) |
下列热化学方程式或离子方程式中,正确的是
| A.甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 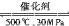 2NH3(g) ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 kJ·mol-1 |
| C.氯化镁溶液与氨水反应:Mg2++2NH3·H2O=Mg(OH)2↓+2NH4+ |
| D.氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O===2Al(OH)3 |
下列热化学方程式正确的是
| A.甲烷的标准燃烧热为 890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890. 3 kJ·mol-1 |
| B.500 ℃、30 MPa 下,将 0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成 NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)⇌2NH3(g) ΔH=-38.6 kJ·mol-1 |
| C.已知在 120 ℃、101 kPa 下,1g H2 燃烧生成水蒸气放出 121 kJ 热量,其热化学方程式为:H2(g)+ |
| D.25 ℃,101 kPa 时,强酸与强碱的稀溶液发生中和反应的中和热为 57.3 kJ/mol,硫酸溶液与氢氧化钡溶液反应的热化学方程式为:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=- 114.6 kJ/mol |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


