解答题-实验探究题 适中0.65 引用1 组卷118
(1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
其他条件不变时:探究温度对化学反应速率的影响,应选择实验_______ (填实验编号); 若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中a和b分别为_______ 和_______ 。
(2)研究表明,SO2催化氧化的反应速率方程为:v = k( −1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v ~ t曲线,如图所示。
−1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v ~ t曲线,如图所示。
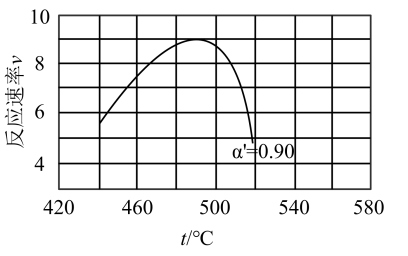
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。下列说法正确的是_______
A.v达到最大值时,SO2平衡转化率α最大
B.t < tm时,v逐渐提高,原因是升高温度,k逐渐增大
C.t > tm后,v逐渐下降,原因是升高温度,α逐渐降低
D.温度是影响反应速率的主要因素,温度越高,反应速率越快
(3)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图2所示:
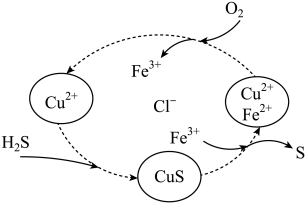
图2
①该循环过程中 Fe3+起的作用是:________ 写出该该反应的化学方程式_______
| 实验 编号 | 实验温 度/℃ | c(Na2S2O3) /(mol·L-1) | V(Na2S2O3) /mL | c(H2SO4) /(mol·L-1) | V(H2SO4) /mL | V(H2O) /mL |
| ① | 25 | 0.1 | 5.0 | 0.1 | 10.0 | a |
| ② | 25 | 0.1 | 10.0 | 0.1 | 10.0 | 0 |
| ③ | 25 | 0.2 | 5.0 | 0.1 | 5.0 | b |
| ④ | 50 | 0.2 | 5.0 | 0.1 | 10.0 | 5.0 |
(2)研究表明,SO2催化氧化的反应速率方程为:v = k(

曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。下列说法正确的是
A.v达到最大值时,SO2平衡转化率α最大
B.t < tm时,v逐渐提高,原因是升高温度,k逐渐增大
C.t > tm后,v逐渐下降,原因是升高温度,α逐渐降低
D.温度是影响反应速率的主要因素,温度越高,反应速率越快
(3)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图2所示:

图2
①该循环过程中 Fe3+起的作用是:
20-21高二上·福建三明·阶段练习
类题推荐
回答下列问题:
(1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
其他条件不变时:探究温度对化学反应速率的影响,应选择实验___________ (填实验编号); 若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中a和b分别为___________ 和___________ 。
(2)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示:
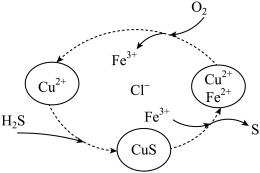
该循环过程中 Fe3+起的作用是:___________ 写出该该反应的化学方程式___________ 。
(3)用H2O2和硫酸共同浸泡印刷电路板制备硫酸铜,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(aq)=CuSO4(aq)+2H2O(l) △H1=-320kJ/mol
又知:2H2O2(l)=2H2O(l)+O2(g) △H2= -196kJ/mol
H2(g)+ O2(g)=H2O(l) △H3= -286kJ/mol
则反应Cu(s)+H2SO4(aq)=CuSO4(aq)+H2(g)的 △H=___________ 。
(1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/(mol·L-1) | V(Na2S2O3)/mL | c(H2SO4)/(mol·L-1) | V(H2SO4)/mL | V(H2O)/mL |
| ① | 25 | 0.1 | 5.0 | 0.1 | 10.0 | a |
| ② | 25 | 0.1 | 10.0 | 0.1 | 10.0 | 0 |
| ③ | 25 | 0.2 | 5.0 | 0.1 | 5.0 | b |
| ④ | 50 | 0.2 | 5.0 | 0.1 | 10.0 | 5.0 |
(2)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示:

该循环过程中 Fe3+起的作用是:
(3)用H2O2和硫酸共同浸泡印刷电路板制备硫酸铜,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(aq)=CuSO4(aq)+2H2O(l) △H1=-320kJ/mol
又知:2H2O2(l)=2H2O(l)+O2(g) △H2= -196kJ/mol
H2(g)+ O2(g)=H2O(l) △H3= -286kJ/mol
则反应Cu(s)+H2SO4(aq)=CuSO4(aq)+H2(g)的 △H=
研究大气中含硫化合物(主要是SO2和H2S)的转化率具有重要意义。
(1)土壤中的微生物可将大气中的H2S经两步反应氧化成 ,两步反应的能量变化示意图如下:
,两步反应的能量变化示意图如下:
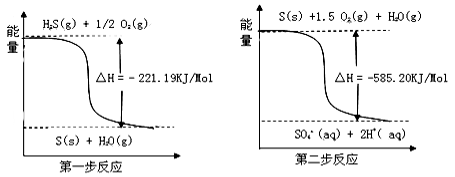
1 mol H2S(g) 全部氧化成 (aq) 的热化学方程式为
(aq) 的热化学方程式为______________________ 。
(2)SO2是工业制硫酸的原料气体之一,一定温度下,向容积为2 L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+ O2(g) 2SO3(g),ΔH = −196 kJ·mol−1,过程中测定的部分数据见表:
2SO3(g),ΔH = −196 kJ·mol−1,过程中测定的部分数据见表:
①反应在0~4min内的平均速率为v(SO2)=___________ ;
②此温度下该反应的化学平衡常数K =_________ ;
③研究表明,SO2催化氧化的反应速率方程为:v = k( −1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v ~ t曲线,如图所示。
−1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v ~ t曲线,如图所示。
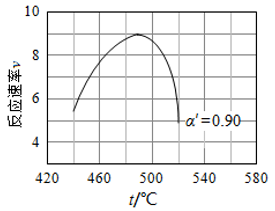
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。下列说法正确的是_______
A.v达到最大值时,SO2平衡转化率α最大
B.t < tm时,v逐渐提高,原因是升高温度,k逐渐增大
C.t > tm后,v逐渐下降,原因是升高温度,α逐渐降低
D.温度是影响反应速率的主要因素,温度越高,反应速率越快
(3)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示:
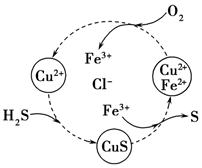
①该循环过程中 Fe3+起的作用是:___________________
②一般来说,如果一个反应的平衡常数大于105,通常认为反应进行得较完全;相反,如果一个反应的平衡常数小于10﹣5,则认为这个反应很难进行.已知常温下各物质的溶度积及电离平衡常数:CuS:Ksp=6.3×10﹣36; H2S:Ka1=1.0×10﹣7,Ka2=7.0×10﹣15,计算反应CuS(s)+ 2H+(aq)= Cu2+(aq)+ H2S(aq)反应的平衡常数K=____________ ,则该反应_______ 进行(填“难”、“易”)。
(1)土壤中的微生物可将大气中的H2S经两步反应氧化成

1 mol H2S(g) 全部氧化成
(2)SO2是工业制硫酸的原料气体之一,一定温度下,向容积为2 L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+ O2(g)
| 时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 0.10 | 0.050 |
| 4 | 0.050 | 0.025 |
| 5 | 0.040 | |
| 8 | 0.020 |
①反应在0~4min内的平均速率为v(SO2)=
②此温度下该反应的化学平衡常数K =
③研究表明,SO2催化氧化的反应速率方程为:v = k(

曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。下列说法正确的是
A.v达到最大值时,SO2平衡转化率α最大
B.t < tm时,v逐渐提高,原因是升高温度,k逐渐增大
C.t > tm后,v逐渐下降,原因是升高温度,α逐渐降低
D.温度是影响反应速率的主要因素,温度越高,反应速率越快
(3)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示:

①该循环过程中 Fe3+起的作用是:
②一般来说,如果一个反应的平衡常数大于105,通常认为反应进行得较完全;相反,如果一个反应的平衡常数小于10﹣5,则认为这个反应很难进行.已知常温下各物质的溶度积及电离平衡常数:CuS:Ksp=6.3×10﹣36; H2S:Ka1=1.0×10﹣7,Ka2=7.0×10﹣15,计算反应CuS(s)+ 2H+(aq)= Cu2+(aq)+ H2S(aq)反应的平衡常数K=
硫代硫酸钠溶液与稀硫酸可发生反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,某同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如表;下列说法正确的是
| 实验编号 | 反应温度/℃ | Na2S2O3 溶液 | 稀 H2SO4 | H2O | ||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
| ① | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ② | 25 | 5 | 0.2 | 5 | 0.1 | 10 |
| ③ | 25 | 5 | 0.1 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.2 | 5 | 0.1 | 10 |
| ⑤ | 50 | 8 | 0.1 | 5 | 0.1 | V1 |
| A.已知实验①10min后沉淀达到最大量,Na2S2O3的反应速率为0.01mol·L-1·min-1 |
| B.其他条件不变时,探究温度对化学反应速率的影响,应选择实验②和实验④ |
| C.选择实验②和实验③,测定混合液变浑浊的时间,可探究硫酸浓度对化学反应速率的影响 |
| D.选择实验④和实验⑤,若可探究Na2S2O3的浓度对反应速率的影响,则V1=10mL |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


