单选题 适中0.65 引用2 组卷204
常温下,向1L0.1mol·L-1NH4Cl溶液中不断加入固体NaOH后,NH 与NH3·H2O 的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是
与NH3·H2O 的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是
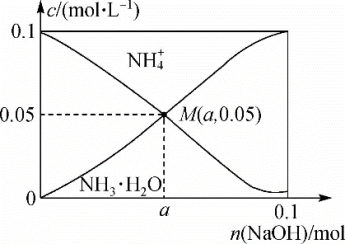

| A.M点溶液中水的电离程度比原溶液大 |
| B.在M点时,n(OH-)-n(H+)=(a +0.05)mol |
| C.当n(NaOH)=0.05mol时,溶液中有:c(Cl-)>c(Na+)>c(NH |
| D.随着NaOH的加入,一定存在c(Cl-)+c(OH-)+c(NH3·H2O)>0.1 mol·L-1 |
21-22高三上·广西河池·期末
类题推荐
室温下,向200mL 0.1 mol•L-1CH3COONa溶液中,逐渐加入0.1 mol•L-1盐酸(不考虑挥发),CH3COOH、CH3COO-物质的量随加入盐酸体积的变化关系如图所示,下列说法正确的是
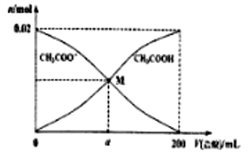
| A.随着盐酸加入,溶液中水的电离程度逐渐增大。 |
| B.随着盐酸加入, |
| C.M 点,n(H+)-n(OH-)=(a×10-4-0.01)mol |
| D.当 V(盐酸)=200mL时,c(CH3COO-)+c(CH3COOH)>c(Cl-) |
常温下,向100mL0.1mol/LNH4Cl溶液中,逐滴滴加0.1mol/LNaOH溶液。NH 和NH3·H2O的变化趋势如图所示(不考虑NH3的逸出)。下列说法错误的是
和NH3·H2O的变化趋势如图所示(不考虑NH3的逸出)。下列说法错误的是
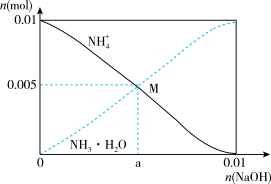

| A.M点溶液中水的电离程度比原溶液小 |
| B.在M点时,n(H+)-n(OH-)=(0.005-a)mol |
| C.随着NaOH溶液的滴加, |
| D.当n(NaOH)=0.01mol时,c(Na+)>c(NH3·H2O)>c(OH-) |
常温下,向1L0.1mol•L-1CH3COONa溶液中,不断通入HCl气体。CH3COO-与CH3COOH 的变化趋势如图所示(假设HCl完全吸收且不考虑CH3COOH挥发及溶液体积变化),下列说法不正确的是


| A.M点溶液中水的电离程度比原溶液小 |
| B.在M点时,n(H+)-n(OH-)=(0.05-a )mol |
C.随着HCl的加入, 不断减小 不断减小 |
| D.当n(HCl)=0.1mol时,c(Cl-)>c(CH3COOH)>c(H+) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


