解答题-原理综合题 适中0.65 引用1 组卷254
CO2的富集与转化有利于降低温室效应。
Ⅰ.CO2的富集:某学习小组设计如图流程:
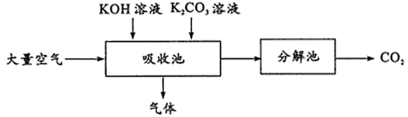
(1)吸收池逸出的气体主要成分是_______ (填化学式,下同),进入分解池中的主要物质是_______ 。
Ⅱ.CO2的转化
(2)①CO2在不同催化剂作用下加氢转化为CO。
已知:CO和H2的燃烧热(△H)分别为 和
和 ,
, △H=-44.0kJ/mol
△H=-44.0kJ/mol
则反应Ⅰ: △H1=
△H1=_______  。
。
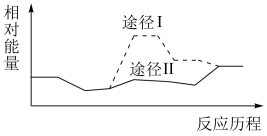
该反应在使用不同催化剂时反应历程与能量变化如图。有关说法正确的是_______ (填序号)
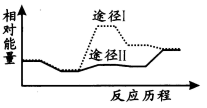
a.反应物总能量高于生成物总能量 b.催化剂能降低反应活化能
c.催化剂能改变反应的焓变 d.途径Ⅱ的反应速率比途径Ⅰ大
②研究表明:在 /
/ 催化剂存在下,CO2和
催化剂存在下,CO2和 反应生成
反应生成 (反应Ⅰ)的同时还可发生反应Ⅱ:
(反应Ⅰ)的同时还可发生反应Ⅱ: △H2=-53.7kJ/mol。
△H2=-53.7kJ/mol。
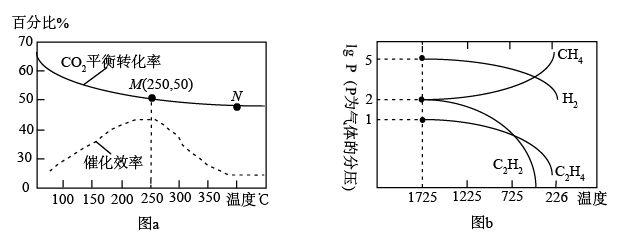
某温度下,按投料比n(CO2):n(H2)=1:3,充入恒容容器进行上述反应,达平衡后缩小容器体积,对反应Ⅰ和反应Ⅱ平衡移动有何影响,分别是_______ ;若随着温度升高,实际测得CO2的平衡转化率与H2的平衡转化率的比值增大,当升高至T℃时其比值接近3,原因可能是_______ 。
Ⅰ.CO2的富集:某学习小组设计如图流程:

(1)吸收池逸出的气体主要成分是
Ⅱ.CO2的转化
(2)①CO2在不同催化剂作用下加氢转化为CO。
已知:CO和H2的燃烧热(△H)分别为
则反应Ⅰ:
该反应在使用不同催化剂时反应历程与能量变化如图。有关说法正确的是

a.反应物总能量高于生成物总能量 b.催化剂能降低反应活化能
c.催化剂能改变反应的焓变 d.途径Ⅱ的反应速率比途径Ⅰ大
②研究表明:在
某温度下,按投料比n(CO2):n(H2)=1:3,充入恒容容器进行上述反应,达平衡后缩小容器体积,对反应Ⅰ和反应Ⅱ平衡移动有何影响,分别是
20-21高二上·四川成都·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网