多选题 适中0.65 引用1 组卷329
由硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO和SiO2)制备绿矾(FeSO4·7H2O)的流程如下,已知:FeS2难溶于水。
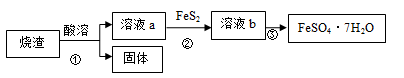
下列说法错误的是

下列说法错误的是
| A.步骤①酸溶烧渣最好选用硫酸 |
| B.步骤②涉及的离子反应为FeS2+16Fe3++8H2O=17Fe2++2SO |
| C.步骤③须控制条件防止氧化 |
| D.将溶液b加热到有较多固体析出,再用余热将液体蒸干得纯净绿矾 |
20-21高一上·山东烟台·期末
类题推荐
由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4•7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如图:

已知:FeS2和铁黄均难溶于水,pH=6.5时,Fe2+易形成Fe(OH)2沉淀。下列说法正确的是
已知:FeS2和铁黄均难溶于水,pH=6.5时,Fe2+易形成Fe(OH)2沉淀。下列说法正确的是
| A.步骤①中,溶解烧渣的酸可以是硫酸、盐酸或者是硝酸 |
| B.步骤②中,涉及的离子方程式为 |
| C.步骤③中,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾 |
| D.步骤④操作时,若反应条件控制不当也不会使铁黄中混有Fe(OH)3 |
由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程:烧渣
 溶液
溶液 绿矾
绿矾 铁黄。已知:FeS2和铁黄均难溶于水。下列说法正确的是
铁黄。已知:FeS2和铁黄均难溶于水。下列说法正确的是
| A.步骤①可用盐酸来溶解烧渣 |
| B.步骤②涉及的离子反应为S2-+8Fe3++4H2O=8Fe2++SO |
| C.步骤③将溶液加热到有少量晶膜出现时停止加热,再冷却结晶析出绿矾 |
| D.步骤④反应条件控制时要让氨气过量,控制强碱性环境,可以提高产品纯度 |
由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:
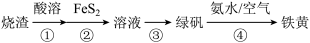
已知:FeS2和铁黄均难溶于水。下列说法不正确的是

已知:FeS2和铁黄均难溶于水。下列说法不正确的是
| A.步骤①,硫酸酸溶后溶液中主要有Fe3+、Fe2+等阳离子 |
| B.步骤②的反应FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+,消耗1molFeS2转移16mol电子 |
| C.步骤③,得到的绿矾晶体久置于空气中会变质 |
| D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


