单选题 适中0.65 引用4 组卷385
某同学设计如图所示实验,探究Fe与稀硝酸、稀硫酸的反应。实验过程中发现①、③中产生的气体在试管口处变为红棕色。
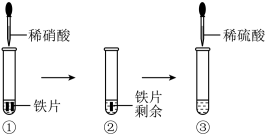
下列说法正确的是

下列说法正确的是
| A.②中大量存在的离子有Fe2+、NO |
| B.①、③产生气体的组成可能不同 |
| C.③溶液中一定既含有Fe2+,又含有Fe3+ |
| D.实验结论:稀硫酸的氧化性大于稀硝酸 |
20-21高一上·山东潍坊·期末
类题推荐
某澄清溶液中可能含有下列离子:K+、NH4+、Fe2+、Fe3+、Ba2+、SO42ˉ、HCO3ˉ、Clˉ,为鉴别其中含有的离子,进行如下实验:
①用玻璃棒蘸取原溶液滴在pH试纸上,试纸显红色;
②另取少量原溶液加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀;
③取②中上层清液加入酸化的硝酸银溶液,生成白色沉淀。
下列关于原溶液的说法正确的是
①用玻璃棒蘸取原溶液滴在pH试纸上,试纸显红色;
②另取少量原溶液加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀;
③取②中上层清液加入酸化的硝酸银溶液,生成白色沉淀。
下列关于原溶液的说法正确的是
| A.原溶液中一定存在SO42ˉ和Clˉ |
| B.取③中滤液加入KSCN,溶液显红色,则原溶液一定有Fe3+ |
| C.原溶液中一定不存在Ba2+和HCO3ˉ |
| D.为确定原溶液中是否含有K+,可通过焰色反应直接观察焰色是否为紫色来确定 |
某澄清溶液中可能含有下列离子中的几种:Na+、NH4+、Fe2+、Fe3+、Ba2+、SO42-、HCO3-、Cl-。对其进行如下实验:
①用玻璃棒蘸取该溶液滴在pH试纸上,试纸显红色;
②另取少量溶液加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀;
③取②中上层清液加入酸化的硝酸银溶液,也生成白色沉淀。
下列关于该溶液的说法中正确的是
①用玻璃棒蘸取该溶液滴在pH试纸上,试纸显红色;
②另取少量溶液加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀;
③取②中上层清液加入酸化的硝酸银溶液,也生成白色沉淀。
下列关于该溶液的说法中正确的是
| A.该溶液中一定不存在Ba2+和HCO3- |
| B.取③中滤液加入KSCN,溶液显血红色,则原溶液中一定有Fe3+ |
| C.该溶液中一定存在SO42-和Cl- |
| D.另取该溶液加入少量稀NaOH溶液,试管口的湿润红色石蕊试纸不变蓝,则原溶液中一定不存在NH4+ |
溶液X中可能含有Fe2+、Ba2+、K+、SO42-、Cl-、CO32-中的某几种,现进行下列实验:
步骤1:取少量溶液,向其中加入足量的NaOH溶液,有白色沉淀生成,沉淀很快变成灰绿色,最终变成红褐色,过滤;
步骤2:向步骤1所得滤液中加入足量BaCl2溶液,有白色沉淀生成,过滤;
步骤3:向步骤2所得滤液中加入足量稀硝酸,再滴加AgNO3溶液,有白色沉淀生成。
下列说法正确的是( )
步骤1:取少量溶液,向其中加入足量的NaOH溶液,有白色沉淀生成,沉淀很快变成灰绿色,最终变成红褐色,过滤;
步骤2:向步骤1所得滤液中加入足量BaCl2溶液,有白色沉淀生成,过滤;
步骤3:向步骤2所得滤液中加入足量稀硝酸,再滴加AgNO3溶液,有白色沉淀生成。
下列说法正确的是( )
| A.步骤1所得白色沉淀为Fe(OH)3 |
| B.溶液X中一定存在的离子有Fe2+、SO42-、Cl- |
| C.溶液X中一定不存在的离子是Ba2+、CO32- |
| D.溶液X中可能存在的离子是K+、Cl-、CO32- |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


