解答题-无机推断题 较易0.85 引用2 组卷172
元素周期表揭示了元素之间的内在联系,使元素构成了一个较为系统的体系.请回答下列问题:
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的_______ 。按照元素在周期表中的顺序给元素编号,得到原子序数。人们发现原子序数与元素的原子结构之间存在如下关系:原子序数=_______ =核外电子数
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。
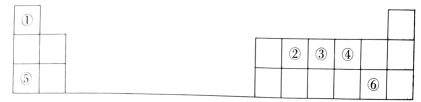
(1)②、③、④三种元素中,原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)①、④、⑤三种元素形成的化合物的电子式为_______ ,该化合物中化学键的类型有_______ 。
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:_______ 。根据元素周期律推测,下列性质中Q不可能具有的是_______ (填选项字母)。
A.最高正化合价为 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。

(1)②、③、④三种元素中,原子半径由大到小的顺序为
(2)①、④、⑤三种元素形成的化合物的电子式为
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:
A.最高正化合价为
20-21高一上·山西·期末
类题推荐
Ⅰ.形式一:(由粒子数推断) 、
、 、
、 、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①
、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:① ;②
;② 。据此,回答下列问题:写出
。据此,回答下列问题:写出 、
、 的化学式:
的化学式:____ 、______ 、
Ⅱ. 形式二:(由元素原子结构推断)A、B、C、D、E、F的原子序数依次增大,它们都是同周期的元素。已知:A、C、F 三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多2。
(1)写出下列元素的符号:A________ ,B________ ,E________
(2)F在元素周期表中的位置为___________________________________
(3)写出C的单质和A的最高价氧化物的水化物反应的离子方程式_______
(4)元素的非金属性为(原子的得电子能力):E________ F(填“强于”或“弱于”),请以E、F为例列举元素非金属性强弱的比较方法__________________________________________________ (至少2条)
通过Ⅱ的解题你认为推断出本题各元素的关键环节为___________
III.形式三:(由元素位置推断)下表为元素周期表的一部分:
请参照元素①-⑧在表中的位置,用化学用语 回答下列问题:
(1)请画出元素⑦的离子结构示意图________________ 。
(2)写出元素⑤在周期表中的位置______________ 。
(3)②、③、⑥的离子半径由大到小的顺序为_________________________ 。
(4)⑤、⑥、⑦的最高价氧化物对应水化物酸性由强到弱的顺序是______ 。
(5)①、②、③三种元素可形成既含离子键又含极性共价键的化合物,写出该化合物的电子式:____________________ 。该化合物与④的最高价氧化物反应的离子方程式为____________________ 。
(6)请你预测:如果发现了原子序数为116号元素,它在周期表中的位置是第________ 周期_______ 族,它属于_____ 元素(填“金属”或“非金属”)
Ⅱ. 形式二:(由元素原子结构推断)A、B、C、D、E、F的原子序数依次增大,它们都是同周期的元素。已知:A、C、F 三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多2。
(1)写出下列元素的符号:A
(2)F在元素周期表中的位置为
(3)写出C的单质和A的最高价氧化物的水化物反应的离子方程式
(4)元素的非金属性为(原子的得电子能力):E
通过Ⅱ的解题你认为推断出本题各元素的关键环节为
III.形式三:(由元素位置推断)下表为元素周期表的一部分:
族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
请参照元素①-⑧在表中的位置,用
(1)请画出元素⑦的离子结构示意图
(2)写出元素⑤在周期表中的位置
(3)②、③、⑥的离子半径由大到小的顺序为
(4)⑤、⑥、⑦的最高价氧化物对应水化物酸性由强到弱的顺序是
(5)①、②、③三种元素可形成既含离子键又含极性共价键的化合物,写出该化合物的电子式:
(6)请你预测:如果发现了原子序数为116号元素,它在周期表中的位置是第
Ⅰ.形式一:(由粒子数推断)A+、B+、C-、D、E5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①A++ C-→D+E;②B++C-→2D。据此,回答下列问题:写出A+、B+的化学式:____________ 、____________ 。
Ⅱ. 形式二:(由元素原子结构推断)A、B、C、D、E、F的原子序数依次增大,它们都是同周期的元素。已知:A、C、F三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多2。
(1)写出下列元素的符号:A________ ,B________ ,E________ 。
(2)F在元素周期表中的位置为___________________________________ 。
(3)写出C的单质和A的最高价氧化物的水化物反应的离子方程式_______ 。
(4)元素的非金属性为(原子的得电子能力):E________ F(填“强于”或“弱于”),请以E、F为例列举元素非金属性强弱的比较方法_________________ 、___________________ (至少2条)。
(学法题)通过Ⅱ的解题你认为推断出本题各元素的关键环节为___________ 。
III.形式三:(由元素位置推断)下表为元素周期表的一部分:
请参照元素①-⑧在表中的位置,用化学用语 回答下列问题:
(1)请画出元素⑦的离子结构示意图________________ 。
(2)写出元素⑤在周期表中的位置______________ 。
(3)②、③、⑥的离子半径由大到小的顺序为_________________________ 。
(4)⑤、⑥、⑦的最高价氧化物对应水化物酸性由强到弱的顺序是______ 。
(5)①、②、③三种元素形成化合物与④的最高价氧化物反应的离子方程式为_________ 。
(6)请你预测:如果发现了原子序数为116号元素,它在周期表中的位置是第________ 周期_______ 族,它属于_____ 元素(填“金属”或“非金属”)。
Ⅱ. 形式二:(由元素原子结构推断)A、B、C、D、E、F的原子序数依次增大,它们都是同周期的元素。已知:A、C、F三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多2。
(1)写出下列元素的符号:A
(2)F在元素周期表中的位置为
(3)写出C的单质和A的最高价氧化物的水化物反应的离子方程式
(4)元素的非金属性为(原子的得电子能力):E
(学法题)通过Ⅱ的解题你认为推断出本题各元素的关键环节为
III.形式三:(由元素位置推断)下表为元素周期表的一部分:
| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)请画出元素⑦的离子结构示意图
(2)写出元素⑤在周期表中的位置
(3)②、③、⑥的离子半径由大到小的顺序为
(4)⑤、⑥、⑦的最高价氧化物对应水化物酸性由强到弱的顺序是
(5)①、②、③三种元素形成化合物与④的最高价氧化物反应的离子方程式为
(6)请你预测:如果发现了原子序数为116号元素,它在周期表中的位置是第
回答下列问题。
Ⅰ、根据①~⑧元素的编号所在周期表中的位置,用相应的元素符号 或者化学用语 回答有关问题:
(1)④、⑤、⑥形成的简单离子的半径由大到小的顺序排列为_______ (用离子符号表示)。
(2)⑦和⑧形成的化合物为X,用电子式表示X的形成过程_______ 。
(3)③的一种核素中子数为9,用原子符号表示该核素为_______ 。
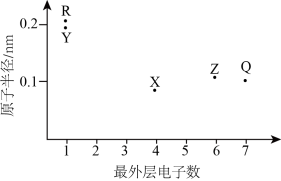
Ⅱ、元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子数之间的关系如图所示。_______ 。
(5)Q元素在周期表中位于第_______ 周期_______ 族;关于Q所在主族的单质及化合物的叙述错误 的是_______ (填标号)。
A.从上到下,单质颜色越来越深,熔、沸点越来越高
B.单质均可与水发生反应生成两种酸
C.单质均具有强氧化性,能将Fe氧化至Fe3+
D.氢化物均易溶于水,且均为强酸
(6)X、Z、Q三种元素的最高价氧化物对应的水化物酸性由强到弱的顺序是_______ (填化学式)。
Ⅰ、根据①~⑧元素的编号所在周期表中的位置,用相应的
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | |||||
| 3 | ⑥ | ⑦ | ⑧ |
(1)④、⑤、⑥形成的简单离子的半径由大到小的顺序排列为
(2)⑦和⑧形成的化合物为X,用电子式表示X的形成过程
(3)③的一种核素中子数为9,用原子符号表示该核素为
Ⅱ、元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子数之间的关系如图所示。
(5)Q元素在周期表中位于第
A.从上到下,单质颜色越来越深,熔、沸点越来越高
B.单质均可与水发生反应生成两种酸
C.单质均具有强氧化性,能将Fe氧化至Fe3+
D.氢化物均易溶于水,且均为强酸
(6)X、Z、Q三种元素的最高价氧化物对应的水化物酸性由强到弱的顺序是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


