解答题-原理综合题 适中0.65 引用1 组卷153
Ⅰ.(1)在101kPa时, 在
在 中完全燃烧生成2mol液态水,放出
中完全燃烧生成2mol液态水,放出 的热量,请写出
的热量,请写出 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(2)已知在常温常压下:①
②
③
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:___________
Ⅱ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。在固定体积的密闭容器中,进行如下化学反应:N2+3H2 2NH3,△H<0,该反应的化学平衡常数表达式是K=
2NH3,△H<0,该反应的化学平衡常数表达式是K=___________ 。已知平衡常数K与温度T的关系如表:
①试判断K1___________ K2(填写“>”“=”或“<”)。
②下列各项能说明该反应已达到平衡状态的是___________ (填字母)。
a.容器内N2、H2、NH3的浓度之比为1∶3∶2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是___________ (填字母)。
a.采用较高温度(400~500℃) b.将生成的氨液化并及时从体系中分离出来
c.用铁触媒加快化学反应速率 d.采用较高压强(20~50MPa)
(2)已知在常温常压下:①
②
③
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
Ⅱ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。在固定体积的密闭容器中,进行如下化学反应:N2+3H2
| T/℃ | 400 | 300 |
| 平衡常数K | K1 | K2 |
①试判断K1
②下列各项能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1∶3∶2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是
a.采用较高温度(400~500℃) b.将生成的氨液化并及时从体系中分离出来
c.用铁触媒加快化学反应速率 d.采用较高压强(20~50MPa)
20-21高二上·广东深圳·期末
类题推荐
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
(1)工业上利用N2和H2可以合成NH3,NH3又可以进一步制备肼(N2H4)等。已知:
N2(g)+2O2(g)=2NO2(g) ΔH=67.7kJ•mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534.0kJ•mol-1
2NO2(g)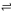 N2O4(g) ΔH=-52.7kJ•mol-1
N2O4(g) ΔH=-52.7kJ•mol-1
写出气态肼在气态四氧化二氮中燃烧生成氨气和气态水的热化学方程式____ 。
(2)在固定体积密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,其平衡常数K与温度T的关系如表:
2NH3(g) ΔH<0,其平衡常数K与温度T的关系如表:
①该反应的平衡常数表达式:K=____ 。
②判断K1____ K2(填写“>”,“=”或“<”)。
③下列各项能说明该反应已达到平衡状态的是____ (填字母)。
a.v(N2)正=3v(H2)逆
b.混合气体的密度保持不变
c.容器内压强保持不变
d.容器内N2、H2、NH3的浓度之比为1︰3︰2
e.N2和H2的转化率相等
f.体系中气体的平均摩尔质量不再改变
(3)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的 ,则该温度下的化学平衡常数K=
,则该温度下的化学平衡常数K=____ (保留两位小数),以NH3表示该过程的反应速率v(NH3)=____ 。
(1)工业上利用N2和H2可以合成NH3,NH3又可以进一步制备肼(N2H4)等。已知:
N2(g)+2O2(g)=2NO2(g) ΔH=67.7kJ•mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534.0kJ•mol-1
2NO2(g)
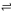 N2O4(g) ΔH=-52.7kJ•mol-1
N2O4(g) ΔH=-52.7kJ•mol-1写出气态肼在气态四氧化二氮中燃烧生成氨气和气态水的热化学方程式
(2)在固定体积密闭容器中,进行如下化学反应:N2(g)+3H2(g)
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×105 | K1 | K2 |
②判断K1
③下列各项能说明该反应已达到平衡状态的是
a.v(N2)正=3v(H2)逆
b.混合气体的密度保持不变
c.容器内压强保持不变
d.容器内N2、H2、NH3的浓度之比为1︰3︰2
e.N2和H2的转化率相等
f.体系中气体的平均摩尔质量不再改变
(3)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
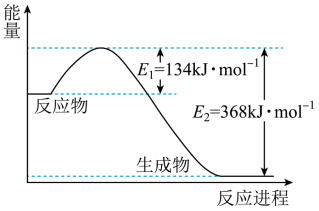
(1)图是1 mol NO2和1 mol CO反应生成CO2 和NO过程中的能量变化示意图,请写出NO2 和CO反应的热化学方程式______________________ 。
(2)在0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
请回答下列问题:
①试比较K1、K2的大小,K1_________ K2(填”>”“=“或”<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是_________ (填序号字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v正(N2)=3v逆(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应2NH3(g) N2(g)+3H2(g)的平衡常数K为
N2(g)+3H2(g)的平衡常数K为______ 。当测得NH3、N2、H2的浓度分别为3 mol • L−1、2 mol • L−1、1 mol • L−1时,则该反应的v正(N2)____ v逆(N2)(填”>”“=“或”<”)

(1)图是1 mol NO2和1 mol CO反应生成CO2 和NO过程中的能量变化示意图,请写出NO2 和CO反应的热化学方程式
(2)在0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
请回答下列问题:
①试比较K1、K2的大小,K1
②下列各项能作为判断该反应达到化学平衡状态的依据是
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v正(N2)=3v逆(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应2NH3(g)
I.研究合成氨反应:N2(g)+3H2(g) 2NH3(g) △H=﹣92.2kJ/mol。
2NH3(g) △H=﹣92.2kJ/mol。
(1)该反应的化学平衡常数表达式是K=_______ 。
(2)该反应的化学平衡常数K与温度T的关系如下表所示:
其中,K1_______ K2(填“>”、“=”或“<”)。
(3)合成氨在农业和国防中有很重要的意义,在实际工作生成中,常采用下列措施,其中可以用勒夏特列原理解释的是_____
①采用较高温度(400℃~500℃) ②采用较高压强(20MPa~50MPa)
③用铁触媒加快化学反应速率 ④将生成的氨液化并及时从体系中分离出来
II.工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l) △H<0,
(1)将2molNH3和1molCO2投到一温度恒定、体积恒定的容器中进行反应,一段时间后可判断该可逆反应达到化学平衡状态的标志是_____ (填字母)。
a.2v正(NH3)=v逆(CO2) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO2、NH3的体积分数均不再变化
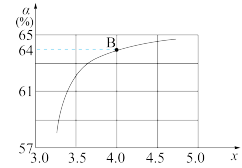
(2)在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比) =x,如图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是
=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是_____ 。图中的B点处,NH3的平衡转化率为_______ 。
(1)该反应的化学平衡常数表达式是K=
(2)该反应的化学平衡常数K与温度T的关系如下表所示:
T/K | 473 | 573 | 673 | … |
K | 4.4×10﹣2 | K1 | K2 | … |
(3)合成氨在农业和国防中有很重要的意义,在实际工作生成中,常采用下列措施,其中可以用勒夏特列原理解释的是
①采用较高温度(400℃~500℃) ②采用较高压强(20MPa~50MPa)
③用铁触媒加快化学反应速率 ④将生成的氨液化并及时从体系中分离出来
II.工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l) △H<0,
(1)将2molNH3和1molCO2投到一温度恒定、体积恒定的容器中进行反应,一段时间后可判断该可逆反应达到化学平衡状态的标志是
a.2v正(NH3)=v逆(CO2) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO2、NH3的体积分数均不再变化
(2)在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


