解答题-工业流程题 适中0.65 引用7 组卷1629
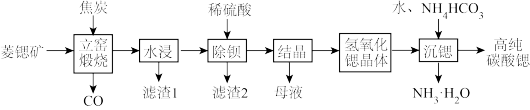
碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如下:
Sr(OH)2在水中的溶解度
(1)元素Sr位于元素周期表第_______ 周期第_______ 族。
(2)菱锶矿、焦炭混合粉碎的目的是_______ 。
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为_______ 。进行煅烧反应的立窑衬里应选择_______ (填“石英砂砖”或“碱性耐火砖”)。
(4)“浸取”中用热水浸取而不用冷水的原因是_______ ;滤渣1含有焦炭、Ca(OH)2和_______ 。
(5)“沉锶”中反应的化学方程式为_______ 。
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则 为
为_______ (取整数)。

Sr(OH)2在水中的溶解度
温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为
(4)“浸取”中用热水浸取而不用冷水的原因是
(5)“沉锶”中反应的化学方程式为
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则
2021·重庆·模拟预测
类题推荐
Ⅰ.手机和笔记本电脑上大面积使用锂离子电池,充电快,使用时间长,功率密度高。工业上常以锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂,工艺流程如下:

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
(1)酸浸时,为了提高浸取率可采取升高温度、粉碎矿石、搅拌等,还可通过___________ 措施来提高浸取率。
(2)反应I中应调节pH范围为___________ ,沉淀A的成分除H2SiO3、CaCO3、Al(OH)3Fe(OH)3外,还有___________
(3)加入H2O2目的是氧化Fe2+为Fe3+(写出对应的离子方程式)___________
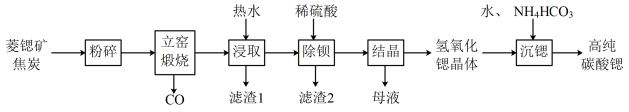
Ⅱ.碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90%SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如下:

Sr(OH)2在水中的溶解度
(4)进行煅烧反应的立窑衬里应选择___________ (填“石英砂砖”或“碱性耐火砖”)。滤渣1含有焦炭和___________
(5)“浸取”中用热水浸取而不用冷水的原因是___________
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则 为
为___________ (取整数)。

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 | 开始沉淀pH | 完全沉淀pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| Mg(OH)2 | 9.6 | 11.0 |
(1)酸浸时,为了提高浸取率可采取升高温度、粉碎矿石、搅拌等,还可通过
(2)反应I中应调节pH范围为
(3)加入H2O2目的是氧化Fe2+为Fe3+(写出对应的离子方程式)
Ⅱ.碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90%SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如下:

Sr(OH)2在水中的溶解度
| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(5)“浸取”中用热水浸取而不用冷水的原因是
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则
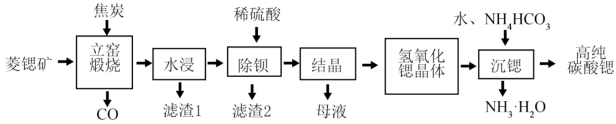
碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(主要含有SrCO3及少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如图所示。
已知:①不溶性碳酸盐高温下分解,生成金属氧化物和CO2,可溶性碳酸盐高温不分解。
②298K时,Ksp[SrCO3]=5.6×10-10、Ksp[CaCO3]=3.36×10-9
③Sr(OH)2在水中的溶解度数据如表:
回答下列问题:
(1)SrCO3中Sr的化合价____ 。
(2)向“立窑煅烧”中投料前,将菱锶矿、焦炭混合粉碎的目的是____ (任写两点)。
(3)“水浸”中用____ (填“冷水”、“热水”),“滤渣1”中含有焦炭、MgO和____ (填化学式)。
(4)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为____ 。
(5)“沉锶”中反应的化学方程式为____ 。
(6)计算298K时,反应CaCO3(s)+Sr2+(aq) SrCO3(s)+Ca2+(aq)平衡常数的数值是
SrCO3(s)+Ca2+(aq)平衡常数的数值是____ 。

已知:①不溶性碳酸盐高温下分解,生成金属氧化物和CO2,可溶性碳酸盐高温不分解。
②298K时,Ksp[SrCO3]=5.6×10-10、Ksp[CaCO3]=3.36×10-9
③Sr(OH)2在水中的溶解度数据如表:
| 温度/℃ | 10 | 60 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 8.42 | 44.5 | 91.2 |
回答下列问题:
(1)SrCO3中Sr的化合价
(2)向“立窑煅烧”中投料前,将菱锶矿、焦炭混合粉碎的目的是
(3)“水浸”中用
(4)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为
(5)“沉锶”中反应的化学方程式为
(6)计算298K时,反应CaCO3(s)+Sr2+(aq)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网