未知-未知 较难0.4 引用0 组卷1159
在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H= -164.7 kJ/mol
CH4(g)+2H2O(g) △H= -164.7 kJ/mol
反应II:CO2(g)+H2(g) CO(g)+H2O(g) △H= 41.2 kJ/mol
CO(g)+H2O(g) △H= 41.2 kJ/mol
反应III:2CO(g)+2H2(g) CO2(g)+CH4(g) △H= -247.1 kJ/mol
CO2(g)+CH4(g) △H= -247.1 kJ/mol
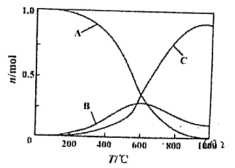
向恒压,密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2 的物质的量随温度的变化如图所示。下列说法正确的是
反应I:CO2(g)+4H2(g)
反应II:CO2(g)+H2(g)
反应III:2CO(g)+2H2(g)
向恒压,密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2 的物质的量随温度的变化如图所示。下列说法正确的是

| A.反应I的平衡常数可表示为K= |
| B.图中曲线B表示CO的物质的量随温度的变化 |
| C.CH4(g)+H2O(g) =CO(g)+3H2(g)的△H= -205.9 kJ/mol |
| D.提高CO2转化为CH4的转化率,需要研发在低温区高效的催化剂 |
类题推荐
CO2催化加氢是碳中和的重要手段之一,以下是CO2加氢时发生的两个主要反应:
反应I:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ΔH1=-165.0 kJ·mol-1
反应II:CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH2
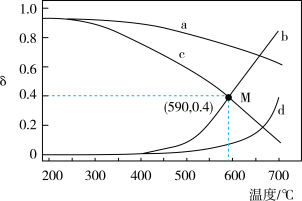
在体积为VL的两个恒容密闭容器中,分别按表所示充入一定量的CO2和H2.平衡体系中 和
和 随温度变化关系如图所示。
随温度变化关系如图所示。
下列有关说法正确的是
反应I:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ΔH1=-165.0 kJ·mol-1
反应II:CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH2
在体积为VL的两个恒容密闭容器中,分别按表所示充入一定量的CO2和H2.平衡体系中
| 容器 | 起始物质的量/mol | |
| CO2 | H2 | |
| 甲 | 0.1 | 0.3 |
| 乙 | 1 | 3 |

下列有关说法正确的是
| A.ΔH2<0 |
| B.曲线b表示乙容器中 |
| C.M点对应H2的总转化率为66.7% |
| D.590℃条件下反应10min,某容器中 |
CH4与CO2催化重整可以同时利用两种温室气体,其工艺过程中涉及如下反应:
反应I:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1=247.4kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=41.2kJ·mol-1
反应Ⅲ:CH4(g)+ O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1
O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1
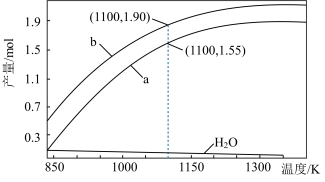
一定条件下,向体积为VL的密闭容器中通入CH4、CO2各1.0mol及少量O2,测得不同温度下反应平衡时各产物产量如图所示。下列说法正确的是
反应I:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1=247.4kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=41.2kJ·mol-1
反应Ⅲ:CH4(g)+
一定条件下,向体积为VL的密闭容器中通入CH4、CO2各1.0mol及少量O2,测得不同温度下反应平衡时各产物产量如图所示。下列说法正确的是

| A.图中曲线b表示H2的平衡产量随温度的变化曲线 |
| B.1100K时,CH4与CO2的转化率分别为95%、90%,反应I的平衡常数 |
| C.反应CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH=206.2kJ·mol-1 |
| D.若选用其它催化剂可能使平衡时H2O的产量随着温度升高而增加 |
CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
反应I:CO2(g)+H2(g) =CO(g)+H2O(g) ΔH=+41.2 kJ·mol−1
反应II:2CO2(g)+6H2(g) =CH3OCH3(g)+3H2O(g) ΔH=—122.5 kJ·mol−1
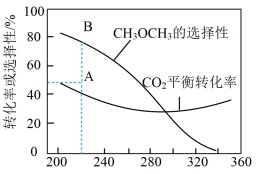
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图所示。 (CH3OCH3的选择性= ×100%)
×100%)
下列说法不正确 的是
反应I:CO2(g)+H2(g) =CO(g)+H2O(g) ΔH=+41.2 kJ·mol−1
反应II:2CO2(g)+6H2(g) =CH3OCH3(g)+3H2O(g) ΔH=—122.5 kJ·mol−1
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图所示。 (CH3OCH3的选择性=

下列说法
| A.CO的选择性随温度的升高逐渐增大 |
| B.反应2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH=—204.9 kJ·mol−1 |
| C.在240~320℃范围内,温度升高,平衡时CH3OCH3的物质的量先增大后减小 |
| D.反应一段时间后,测得CH3OCH3的选择性为48%(图中A点),增大压强可能将CH3OCH3的选择性提升到B点 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


