解答题-工业流程题 较难0.4 引用8 组卷2406
综合利用炼锌矿渣(主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4)获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如下:
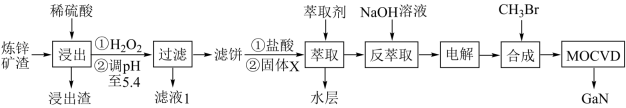
已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表2。
表1金属离子浓度及开始沉淀的pH
表2金属离子的萃取率
(1)Ga2(Fe2O4)3中Ga的化合价为______ ,“浸出”时其发生反应的离子方程式为______ 。
(2)滤液1中可回收利用的物质是______ ,滤饼的主要成分是______ ;萃取前加入的固体X为______ 。
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为______ (填化学式)。
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极的电极反应为______ 。
(5)GaN可采用MOCVD (金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为______ 。
(6)滤液1中残余的Ga3+的浓度为______ mol·L-1 (写出计算过程)。

已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表2。
表1金属离子浓度及开始沉淀的pH
| 金属离子 | 浓度(mol·L-1) | 开始沉淀pH |
| Fe2+ | 1.0×10-3 | 8.0 |
| Fe3+ | 4.0×10-2 | 1.7 |
| Zn2+ | 1.5 | 5.5 |
| Ga3+ | 3.0×10-3 | 3.0 |
| 金属离子 | 萃取率(%) |
| Fe2+ | 0 |
| Fe3+ | 99 |
| Zn2+ | 0 |
| Ga3+ | 97-98.5 |
(2)滤液1中可回收利用的物质是
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极的电极反应为
(5)GaN可采用MOCVD (金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为
(6)滤液1中残余的Ga3+的浓度为
2021·广东·模拟预测
类题推荐
金属镓拥有电子工业脊梁的美誉,镓与铝同族,化学性质相似。综合利用炼锌矿渣[主要含铁酸嫁 、铁酸锌
、铁酸锌 ]获得3种金属盐,并利用镓盐电解制备金属镓,部分工艺流程如下:
]获得3种金属盐,并利用镓盐电解制备金属镓,部分工艺流程如下:
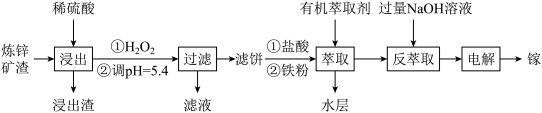
已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见下表:
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见下表:
回答下列问题:
(1) 中的
中的 化合价为
化合价为_______ 。“浸出”时 矿渣经过硫酸浸出获得2种金属盐,该反应的离子方程式为
矿渣经过硫酸浸出获得2种金属盐,该反应的离子方程式为_______ 。
(2)“过滤”后滤液中可回收利用的物质是_______ 。滤饼的主要成分是_______ (填化学式)。
(3)滤液中残余的 的浓度为
的浓度为_______  。
。
(4)“萃取”前加入的 的目的是
的目的是_______ 。
(5)“反萃取”时镓元素发生反应的离子方程式_______ 。
(6)“电解”过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以 溶液为电解液,阴极的电极反应式为
溶液为电解液,阴极的电极反应式为_______ 。

已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见下表:
| 金属离子 | ||||
| 浓度( | 1.5 | |||
| 开始沉淀pH | 8.0 | 1.7 | 5.5 | 3.0 |
| 金属离子 | ||||
| 萃取率(%) | 0 | 99 | 0 | 97-98.5 |
(1)
(2)“过滤”后滤液中可回收利用的物质是
(3)滤液中残余的
(4)“萃取”前加入的
(5)“反萃取”时镓元素发生反应的离子方程式
(6)“电解”过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以
综合利用炼锌矿渣(主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4)获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图:

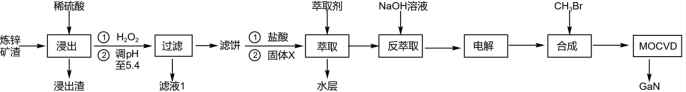
已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表2。
表1金属离子浓度及开始沉淀的pH
表2金属离子的萃取率
滤液1中残余的Ga3+的浓度为_______ mol·L-1 (写出计算过程)。

已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表2。
表1金属离子浓度及开始沉淀的pH
| 金属离子 | 浓度(mol·L-1) | 开始沉淀pH |
| Fe2+ | 1.0×10-3 | 8.0 |
| Fe3+ | 4.0×10-2 | 1.7 |
| Zn2+ | 1.5 | 5.5 |
| Ga3+ | 3.0×10-3 | 3.0 |
表2金属离子的萃取率
| 金属离子 | 萃取率(%) |
| Fe2+ | 0 |
| Fe3+ | 99 |
| Zn2+ | 0 |
| Ga3+ | 97-98.5 |
滤液1中残余的Ga3+的浓度为
综合处理炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4],实现变废为宝得到多种产品,进一步利用镓盐可制备具有优异光电性能的氮化镓GaN(Ga与Al同主族),部分工艺流程如图:
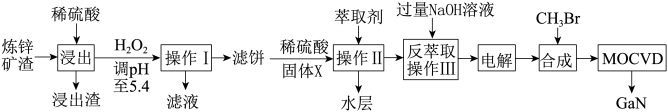
已知:①常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表:
②当溶液中剩余离子的浓度小于10-5mol·L-1时,视为沉淀完全。
③MOCVD:化学气相沉积,以合成的三甲基镓为原料,使其与NH3反应得到GaN。
请回答下列问题:
(1)已知铁酸锌可以用ZnO·Fe2O3表示,写出浸出时铁酸锌参加反应的化学方程式____ 。
(2)浸出后调节pH至5.4的目的是____ 。
(3)固体X最佳选择为____ ,电解过程可得粗镓,则得到金属镓的电极反应式为____ 。
(4)三甲基镓与NH3反应得到GaN的同时获得的副产物为____ 。
(5)滤液中残留的镓离子的浓度为____ mol·L-1。由滤液可制备ZnC2O4·2H2O,再通过热分解探究其产物,制备ZnC2O4·2H2O时,为提高晶体的纯度,Na2C2O4溶液和滤液混合时应将____ 加入到____ 中,已知ZnC2O4·2H2O的TG-DTA(热重分析一差热分析)曲线如图所示。

则ZnC2O4·2H2O分解是____ 反应(填“放热”或“吸热”),分解的总化学方程式为____ 。

已知:①常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表:
| 金属离子 | Fe2+ | Fe3+ | Zn2+ | Ga3+ |
| 开始沉淀pH | 8.0 | 1.7 | 5.5 | 3.0 |
| 沉淀完全pH | 9.6 | 3.2 | 8.0 | 4.9 |
| 萃取率(%) | 0 | 99 | 0 | 97~98.5 |
③MOCVD:化学气相沉积,以合成的三甲基镓为原料,使其与NH3反应得到GaN。
请回答下列问题:
(1)已知铁酸锌可以用ZnO·Fe2O3表示,写出浸出时铁酸锌参加反应的化学方程式
(2)浸出后调节pH至5.4的目的是
(3)固体X最佳选择为
(4)三甲基镓与NH3反应得到GaN的同时获得的副产物为
(5)滤液中残留的镓离子的浓度为

则ZnC2O4·2H2O分解是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


