解答题-实验探究题 较难0.4 引用2 组卷461
某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如图所示:
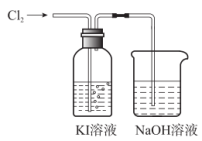
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)Cl2与NaOH溶液反应的化学方程式是_______ ;
(2)KI溶液变为黄色说明氯气具有_______ 性,该反应的离子方程式是_______ ;
(3)已知 ,
, 、
、 在水中均呈黄色。为确定黄色溶液的成分,进行以下实验:
在水中均呈黄色。为确定黄色溶液的成分,进行以下实验:
①实验b的目的是_______ ;
②根据实验a可知,水层中含有的粒子有_______ ;
③用化学平衡原理解释实验a中水溶液颜色变浅的原因:_______ ;
(4)通入氯气,溶液由黄色变为无色,是因为氯气将 氧化。已知
氧化。已知 可氧化
可氧化 ,该反应的离子方程式是
,该反应的离子方程式是_______ ;
(5)根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为_______ ;
(6)溶液最终变为浅黄绿色的原因是_______ 。

通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)Cl2与NaOH溶液反应的化学方程式是
(2)KI溶液变为黄色说明氯气具有
(3)已知
| 操作 | 实验现象 | |
| a | 取2~3mL黄色溶液,加入足量 | |
| b | 取2~3mL饱和碘水,加入足量 |
②根据实验a可知,水层中含有的粒子有
③用化学平衡原理解释实验a中水溶液颜色变浅的原因:
(4)通入氯气,溶液由黄色变为无色,是因为氯气将
(5)根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为
(6)溶液最终变为浅黄绿色的原因是
21-22高三上·北京通州·期末
类题推荐
某小组同学探究I2能否将Fe2+氧化为Fe3+。
试管中加适量铁粉,加入10 mL稀盐酸,充分反应后,铁粉有少量剩余,取适量上层清液于试管中,滴加少量棕黄色的碘水,振荡试管观察到溶液变为黄色。
(1)小组同学认为试管中溶液呈黄色不能说明I2将Fe2+氧化为Fe3+,其理由是:________ 。
(2)继续进行实验
①试管中加入CCl4的目的是________ 。
②滴加KSCN溶液后,溶液变成浅红色的原因是________ 。
(3)有同学认为该实验现象不能说明I2将Fe2+氧化为Fe3+,理由是___ 。
(4)经查阅资料,发现Cl2和Br2都能将Fe2+ 氧化,请写出Cl2与Fe2+ 反应的离子方程式为________ ;I2与FeCl2溶液反应的程度很小。
(5)Cl2、Br2、I2氧化Fe2+的能力逐渐减弱,从原子结构解释其原因_______ 。
试管中加适量铁粉,加入10 mL稀盐酸,充分反应后,铁粉有少量剩余,取适量上层清液于试管中,滴加少量棕黄色的碘水,振荡试管观察到溶液变为黄色。
(1)小组同学认为试管中溶液呈黄色不能说明I2将Fe2+氧化为Fe3+,其理由是:
(2)继续进行实验
操作 | 现象 |
| 向试管中继续加入0.5 mL CCl4,充分振荡,静置 | 静置后,上层溶液几乎无色,下层溶液为紫色 |
| 取出上层溶液,滴加KSCN溶液 | 溶液变成浅红色 |
②滴加KSCN溶液后,溶液变成浅红色的原因是
(3)有同学认为该实验现象不能说明I2将Fe2+氧化为Fe3+,理由是
(4)经查阅资料,发现Cl2和Br2都能将Fe2+ 氧化,请写出Cl2与Fe2+ 反应的离子方程式为
(5)Cl2、Br2、I2氧化Fe2+的能力逐渐减弱,从原子结构解释其原因
某兴趣小组对Fe3+与I-的反应进行探究。
Ⅰ.室温下进行下表所列实验。
试填空:
(1)实验2证明实验1中有I2生成,加入的试剂是___________ ,实验现象是___________ 。
(2)上述实验可以证明Fe3+与I-发生可逆反应,原因是___________ 。
(3)实验1中Fe3+与I-反应的离子方程式为___________ 。
Ⅱ.20min后,观察到实验1所得溶液棕黄色变深(标记为溶液b)。小组同学继续对溶液颜色变化的原因进行探究。
查阅资料:i.I-+I2 I
I ,I
,I 呈棕褐色。I-、I
呈棕褐色。I-、I 难溶于CCl4;
难溶于CCl4;
ii.在酸性较强的条件下,I-可被空气氧化为I2.
(4)提出假设:
假设1:溶液中生成了___________ 。
假设2:空气将溶液中的I-氧化为I2,c(I2)增大。补全该反应的离子方程式。
4I-+O2+___________ =I2+___________
(5)设计并进行实验。
①证明假设1成立的实验现象是___________ 。
②实验6证明假设2不成立,其实验操作是___________ 。该实验中,20min后溶液不变蓝的原因可能是___________ (写出一条即可)。
Ⅰ.室温下进行下表所列实验。
| 序号 | 实验操作 | 实验现象 |
| 实验1 | 向5mL0.1mol·L-1KI溶液中,加入5滴0.1mol·L-1FeCl3溶液(混合溶液pH=5) | 溶液变为棕黄色(标记为溶液a) |
| 实验2 | 取1mL溶液a,加入___________ | ___________ |
| 实验3 | 取1mL溶液a,滴加2滴0.1mol·L-1KSCN溶液 | 溶液变红 |
(1)实验2证明实验1中有I2生成,加入的试剂是
(2)上述实验可以证明Fe3+与I-发生可逆反应,原因是
(3)实验1中Fe3+与I-反应的离子方程式为
Ⅱ.20min后,观察到实验1所得溶液棕黄色变深(标记为溶液b)。小组同学继续对溶液颜色变化的原因进行探究。
查阅资料:i.I-+I2
ii.在酸性较强的条件下,I-可被空气氧化为I2.
(4)提出假设:
假设1:溶液中生成了
假设2:空气将溶液中的I-氧化为I2,c(I2)增大。补全该反应的离子方程式。
4I-+O2+
(5)设计并进行实验。
| 序号 | 实验操作 | 实验现象 |
| 实验4 | 取1mL与溶液b颜色相近的碘水,加入1mLCCl4,振荡后静置 | 水层几近无色 |
| 实验5 | 取1mL溶液b,加入1mLCCl4,振荡相同时间后静置 | 水层显浅黄色 |
| 实验6 | ___________ | 20min后溶液不变蓝 |
②实验6证明假设2不成立,其实验操作是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



