解答题-实验探究题 较难0.4 引用2 组卷941
碘是人体必需的微量元素,也可用于工业、医药等领域。大量的碘富集于海藻灰〔主要成分是 )中,因此从海藻灰中提取碘,可有效利用海洋资源。
)中,因此从海藻灰中提取碘,可有效利用海洋资源。
(1)某兴趣小组以海藻灰为原料进行 的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了
的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了 溶液,将适量
溶液,将适量 固体溶于
固体溶于 溶液,再将
溶液,再将 饱和溶液滴入上述溶液中,生成白色
饱和溶液滴入上述溶液中,生成白色 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为______ 。
(2)待 沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓
沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓 ,观察到
,观察到______ (颜色)气体放出,______ (颜色)晶体析出。出于安全和环保考虑,该实验操作需在______ (条件)下进行。该反应的化学方程式为______ 。
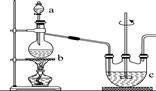
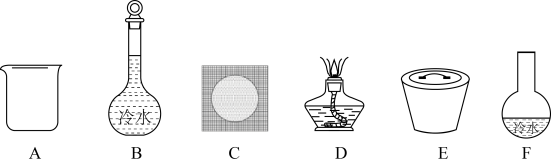
(3)用倾析法弃去上清液,固体物质用少量水洗涤后得到粗 ,进一步精制时,选择必需的仪器搭建装置,并按次序排列:
,进一步精制时,选择必需的仪器搭建装置,并按次序排列:______ (夹持装置略)。
(4)将精制得到的 配成浓度为
配成浓度为 的标准溶液,用来测定某样品中维生素C(相对分子质量为M的含量。具体操作如下:准确称量ag样品,溶于新煮沸过并冷却至室温的蒸馏水中,煮沸蒸馏水的目的是
的标准溶液,用来测定某样品中维生素C(相对分子质量为M的含量。具体操作如下:准确称量ag样品,溶于新煮沸过并冷却至室温的蒸馏水中,煮沸蒸馏水的目的是______ 。用 容量瓶定容,使用
容量瓶定容,使用______ (仪器)量取 样品溶液于锥形瓶中,再加入
样品溶液于锥形瓶中,再加入 1∶1醋酸溶液和适量的
1∶1醋酸溶液和适量的______ 指示剂,立即用 标准溶液滴定,溶液显稳定的
标准溶液滴定,溶液显稳定的______ (颜色)即为滴定终点,消耗 标准溶液
标准溶液 ,则样品中维生素C的质量分数是
,则样品中维生素C的质量分数是______ (写出表达式)。已知滴定反应方程式:
(1)某兴趣小组以海藻灰为原料进行
(2)待
(3)用倾析法弃去上清液,固体物质用少量水洗涤后得到粗

(4)将精制得到的

2021·河北·模拟预测
类题推荐
某学习小组按如下实验流程探究海带中碘含量的测定和单质碘的制取与应用。
实验(一) 碘含量的测定
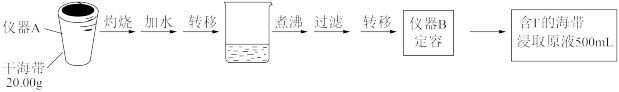
取0.0100 的AgNO3标准溶液装入滴定管,取100.00mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E)反映溶液中
的AgNO3标准溶液装入滴定管,取100.00mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E)反映溶液中 的变化,部分数据如下表:
的变化,部分数据如下表:
请回答:
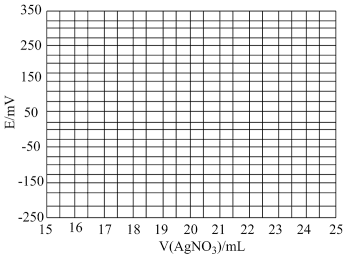
(1)①根据表中数据绘制滴定曲线:___________
②该次滴定终点时用去AgNO3溶液的体积为___________ mL,计算得海带中碘的百分含量为___________ %。
实验(二) 维生素C含量的测定
(2)将精制得到的I2配成浓度为 的标准溶液,用来测定某样品中维生素C(相对分子质量为M)的含量。具体操作如下:准确称量ag样品,溶于新煮沸过并冷却至室温的蒸馏水中,煮沸蒸馏水的目的是
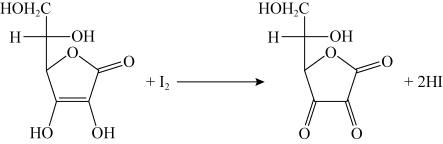
的标准溶液,用来测定某样品中维生素C(相对分子质量为M)的含量。具体操作如下:准确称量ag样品,溶于新煮沸过并冷却至室温的蒸馏水中,煮沸蒸馏水的目的是___________ 。用250mL容量瓶定容,使用___________ (填仪器)量取25.00mL样品溶液于锥形瓶中,再加入10mL1:1醋酸溶液和适量的___________ 指示剂,立即用I2标准溶液滴定,溶液显稳定的___________ (填颜色)即为滴定终点,消耗I2标准溶液VmL,则样品中维生素C的质量分数是____ (写出表达式)。已知滴定反应方程式:  +I2
+I2
 +2HI
+2HI
实验(一) 碘含量的测定
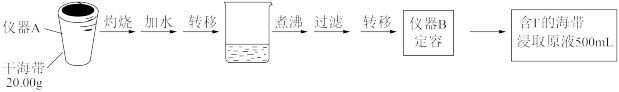
取0.0100
| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | 50.0 | 175 | 275 | 300 | 325 |

(1)①根据表中数据绘制滴定曲线:
②该次滴定终点时用去AgNO3溶液的体积为
实验(二) 维生素C含量的测定
(2)将精制得到的I2配成浓度为
 +I2
+I2 +2HI
+2HI 组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网