解答题-工业流程题 适中0.65 引用1 组卷287
叠氨化钠(NaN3)是汽车安全气囊最理想的气体发生剂原料。下面是工业水合肼法制备叠氮化钠的工艺流程:
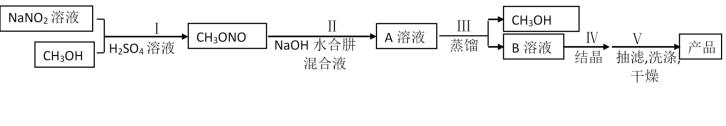
已知 能与
能与 反应生成白色难溶于水的
反应生成白色难溶于水的 ;有关物质的物理性质如下表:
;有关物质的物理性质如下表:
请回答:
(1)步骤Ⅰ中 与稀硫酸发生副反应生成两种气体(其中一种气体在空气中可以转化为另一种气体)的离子方程式为
与稀硫酸发生副反应生成两种气体(其中一种气体在空气中可以转化为另一种气体)的离子方程式为___________ 。
(2)实验室模拟步骤Ⅱ实验装置如下图(装置中冷却水省略,下同):

①仪器a的名称___________ 。
②根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是___________ 。
③图中X处连接的最合适装置应为下图中的___________ (填标号)。

(3)步骤Ⅱ、Ⅲ中制备叠氮化钠并对溶液A进行蒸馏的合理操作顺序是___________ 。
①打开 、
、 ,关闭
,关闭 ②打开
②打开 ③加热④关闭
③加热④关闭 、
、
(4)步骤Ⅳ对溶液B加热蒸发至溶液体积的三分之一, 结晶析出。
结晶析出。
①步骤V可以用___________ 洗涤晶体。
A.水 B.乙醇 C.乙醇水溶液 D.乙醚
②沉淀滴定法测定产品纯度,是以淡黄色 溶液作指示剂,将
溶液作指示剂,将 标准溶液滴入样品溶液,至有少量
标准溶液滴入样品溶液,至有少量 出现,即溶液呈淡红色为终点。下列操作或说法合理的是
出现,即溶液呈淡红色为终点。下列操作或说法合理的是___________ (填标号)。
A.滴定管和移液管管尖不可接触锥形瓶内壁
B.滴定时滴液速度应先快后慢,接近终点时一滴一摇
C.滴定过程中可用蒸馏水将锥形瓶壁上粘附的溶液冲下
D.若未等滴定管液面稳定就读数会导致测定结果偏高
E.若发现滴液过量,可回滴样品溶液,至红色褪去

已知
| 熔点 | 沸点 | 溶解性 | |
| 64.7 | 与水互溶 | ||
| 水合肼( | 2 | 113.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
| 亚硝酸甲酯( | 溶于乙醚、氯仿 |
请回答:
(1)步骤Ⅰ中
(2)实验室模拟步骤Ⅱ实验装置如下图(装置中冷却水省略,下同):

①仪器a的名称
②根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是
③图中X处连接的最合适装置应为下图中的

(3)步骤Ⅱ、Ⅲ中制备叠氮化钠并对溶液A进行蒸馏的合理操作顺序是
①打开
(4)步骤Ⅳ对溶液B加热蒸发至溶液体积的三分之一,
①步骤V可以用
A.水 B.乙醇 C.乙醇水溶液 D.乙醚
②沉淀滴定法测定产品纯度,是以淡黄色
A.滴定管和移液管管尖不可接触锥形瓶内壁
B.滴定时滴液速度应先快后慢,接近终点时一滴一摇
C.滴定过程中可用蒸馏水将锥形瓶壁上粘附的溶液冲下
D.若未等滴定管液面稳定就读数会导致测定结果偏高
E.若发现滴液过量,可回滴样品溶液,至红色褪去
21-22高三上·湖南长沙·阶段练习
类题推荐
工业水合肼法制备叠氮化钠的工艺流程如图所示:

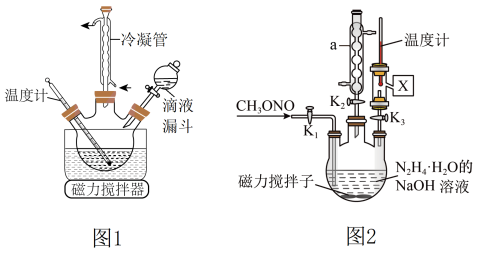
一、合成水合肼
已知: (水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。
(水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。 (水合肼)熔点-40℃,沸点118.5℃。
(水合肼)熔点-40℃,沸点118.5℃。
合成 的装置如图1所示。
的装置如图1所示。 碱性溶液与尿素
碱性溶液与尿素 水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
(1)写出 的结构式
的结构式____________ , 的电子式
的电子式____________
(2)①写出制取 的离子方程式
的离子方程式___________________________
②实验中通过滴液漏斗滴加的溶液是_________ 理由是_______________ 图1使用冷凝管的目的是____________________________________
③从反应后的混合溶分离出 ,应该采用的分离方法最合理的是
,应该采用的分离方法最合理的是________ 。
二、合成叠氮化钠( )晶体
)晶体
已知:相关物质的物理性质如下表
(3)实验室模拟工艺流程步骤Ⅱ的实验装置如图2
①根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是________________ 。(写出1点即可)
②图中 处连接的最合适装置应为下图中的
处连接的最合适装置应为下图中的__________ 。
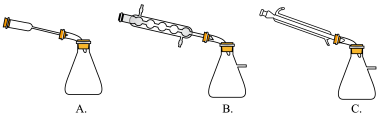
③步骤Ⅱ中制备叠氮化钠的操作是________ (填序号)步骤Ⅲ中溶液 进行蒸馏的合理操作顺序是
进行蒸馏的合理操作顺序是_______ 。(填序号)
①打开 ,关闭
,关闭 ②打开
②打开 ③加热④关闭
③加热④关闭
(4)步骤Ⅳ对溶液 加热蒸发至溶液体积的
加热蒸发至溶液体积的 ,
, 结晶析出。步骤Ⅴ可以用
结晶析出。步骤Ⅴ可以用________ 洗涤晶体。
A.水B.乙醚C.乙醇水溶液D.乙醇
(5)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:
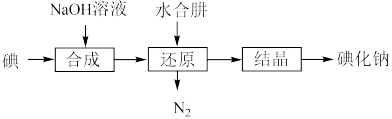
还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是______________________________________ 。


一、合成水合肼
已知:
合成
(1)写出
(2)①写出制取
②实验中通过滴液漏斗滴加的溶液是
③从反应后的混合溶分离出
二、合成叠氮化钠(
已知:相关物质的物理性质如下表
| 熔点℃ | 沸点℃ | 溶解性 | |
| -97 | 67.1 | 与水互溶 | |
| 水合肼( | -40 | 118.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
| 亚硝酸甲酯( | -17 | -12 | 溶于乙醇、乙醚 |
| NaN3 | 与水互溶,不溶于乙醚、微溶于乙醇 |
(3)实验室模拟工艺流程步骤Ⅱ的实验装置如图2
①根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是
②图中

③步骤Ⅱ中制备叠氮化钠的操作是
①打开
(4)步骤Ⅳ对溶液
A.水B.乙醚C.乙醇水溶液D.乙醇
(5)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:

还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是
叠氮化钠(NaN3)是汽车安全气囊最理想的气体发生剂原料。水合肼法制备叠氮化钠的工艺流程如下:
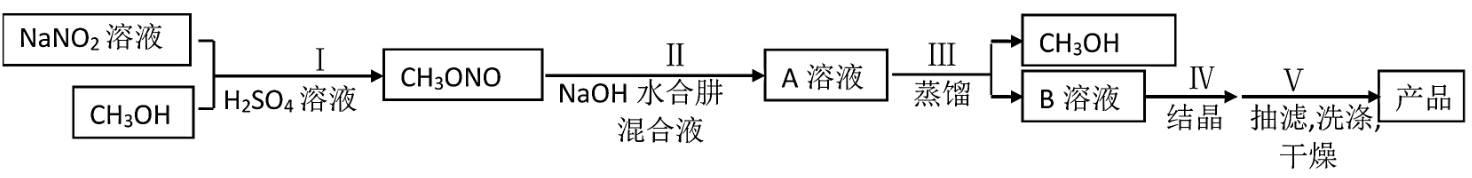
i)有关物质的物理性质如下表:
ii)步骤Ⅱ中生成NaN3的原理:CH3ONO+N2H4·H2O+NaOH=CH3OH+NaN3+3H2O
请回答:
(1)步骤Ⅰ中NaNO2与稀硫酸发生副反应生成两种气体的离子方程式为___________ 。
(2)图1装置中多孔球泡的作用是___________ ;操作Ⅲ的名称为___________ 。
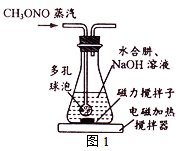
(3)步骤Ⅳ对溶液B加热蒸发至溶液体积的1/3,NaN3结晶析出;步骤Ⅴ洗涤晶体可以用___________
A.水 B.乙醇 C.乙醇水溶液 D.乙醚
(4)步骤V采用抽滤,下列关于抽滤的说法正确的是___________

A.滤纸应比漏斗内径略小,且能盖住所有小孔
B.图2抽滤装置中只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
C.抽滤得到的滤液应从吸滤瓶的支管口倒出
D.抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒吸
(5)测定NaN3产品纯度:
①称取NaN3产品5.000g,用适量稀硫酸溶解后配成100.0mL溶液A;
②取25.00mL溶液A,加入20.00mL0.2000 mol·L-1KMnO4溶液,得紫红色溶液B;
③向溶液B中加入足量KI溶液,以消耗过量的KMnO4溶液,然后以淀粉作指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定产生的I2,消耗Na2S2O3溶液30.00mL。
测定过程中物质的转化关系如下:
10NaN3+2KMnO4+8H2SO4=2MnSO4+K2SO4+5Na2SO4+8H2O+15N2↑;
10I- + 2MnO + 16H+ = 5I2 + 2Mn2+ + 8H2O;
+ 16H+ = 5I2 + 2Mn2+ + 8H2O;
I2 + 2S2O =2I- + S4O
=2I- + S4O 。
。
则NaN3产品的纯度为___________ ;滴定到终点时俯视读数,会导致测定结果___________ (填“偏高”、“偏低”或“无影响”)。

i)有关物质的物理性质如下表:
| 熔点℃ | 沸点℃ | 溶解性 | |
| CH3OH | -97 | 64.7 | 与水互溶 |
| 水合肼(N2H4·H2O) | 2 | 113.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
| 亚硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇、乙醚 |
| 叠氮化钠(NaN3) | 410(易分解) | - | 易溶于水,难溶于醇,不溶于乙醚 |
请回答:
(1)步骤Ⅰ中NaNO2与稀硫酸发生副反应生成两种气体的离子方程式为
(2)图1装置中多孔球泡的作用是

(3)步骤Ⅳ对溶液B加热蒸发至溶液体积的1/3,NaN3结晶析出;步骤Ⅴ洗涤晶体可以用
A.水 B.乙醇 C.乙醇水溶液 D.乙醚
(4)步骤V采用抽滤,下列关于抽滤的说法正确的是

A.滤纸应比漏斗内径略小,且能盖住所有小孔
B.图2抽滤装置中只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
C.抽滤得到的滤液应从吸滤瓶的支管口倒出
D.抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒吸
(5)测定NaN3产品纯度:
①称取NaN3产品5.000g,用适量稀硫酸溶解后配成100.0mL溶液A;
②取25.00mL溶液A,加入20.00mL0.2000 mol·L-1KMnO4溶液,得紫红色溶液B;
③向溶液B中加入足量KI溶液,以消耗过量的KMnO4溶液,然后以淀粉作指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定产生的I2,消耗Na2S2O3溶液30.00mL。
测定过程中物质的转化关系如下:
10NaN3+2KMnO4+8H2SO4=2MnSO4+K2SO4+5Na2SO4+8H2O+15N2↑;
10I- + 2MnO
I2 + 2S2O
则NaN3产品的纯度为
叠氮化钠(NaN3)常用作汽车安全气囊及头孢类药物生产等。水合肼还原亚硝酸甲酯(CH3ONO)制备叠氮化钠(NaN3)的工艺流程如下:
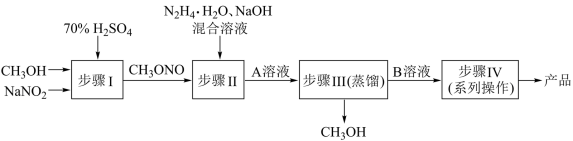
已知:i.叠氮化钠受热或剧烈撞击易分解,具有较强的还原性。
ii.相关物质的物理性质如下表:
(1)步骤I总反应的化学方程式为___________ 。
(2)实验室模拟工艺流程步骤II、III的实验装置如图。
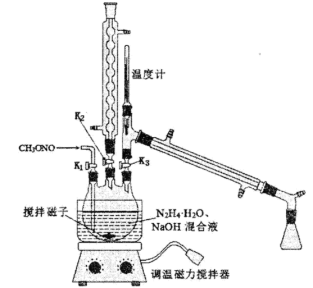
①步骤II三颈烧瓶中发生反应的化学方程式为___________ 。该反应放热,但在20℃左右选择性和转化率最高,实验中控制温度除使用冷水浴,还需采取的措施是___________ 。
②步骤II开始时的操作为___________ (选填字母编号)。步骤III蒸馏时的操作顺序是___________ (选填字母编号)。
a.打开K1、K2 b.关闭K1、K2 c.打开K3 d.关闭K3 e.水浴加热 f.通冷凝水
(3)步骤IV对B溶液加热蒸发至溶液体积的三分之一,冷却析出NaN3晶体,减压过滤,晶体用乙醇洗涤2~3次后,再___________ 干燥。精制NaN3的方法是___________ 。
(4)实验室用滴定法测定产品纯度。测定过程涉及的反应为:
2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑
Ce4++Fe2+=Ce3++Fe3+
称取2.50 g产品配成250 mL溶液,取25.00 mL置于锥形瓶中,加入V1 mLc1 mol·L-1(NH4)2Ce(NO3)6溶液,充分反应后稍作稀释,向溶液中加适量硫酸,滴加2滴邻菲罗啉指示剂,用c2 mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗标准溶液V2 mL。
①产品纯度为___________ 。
②为了提高实验的精确度,该实验还需要___________ 。

已知:i.叠氮化钠受热或剧烈撞击易分解,具有较强的还原性。
ii.相关物质的物理性质如下表:
| 相关物质 | 熔点℃ | 沸点℃ | 溶解性 |
| CH3OH | -97 | 67.1 | 与水互溶 |
| 亚硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇、乙醚 |
| 水合肼(N2H4·H2O) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
| NaN3 | 275 | 300 | 与水互溶,微溶于乙醇,不溶于乙醚 |
(2)实验室模拟工艺流程步骤II、III的实验装置如图。

①步骤II三颈烧瓶中发生反应的化学方程式为
②步骤II开始时的操作为
a.打开K1、K2 b.关闭K1、K2 c.打开K3 d.关闭K3 e.水浴加热 f.通冷凝水
(3)步骤IV对B溶液加热蒸发至溶液体积的三分之一,冷却析出NaN3晶体,减压过滤,晶体用乙醇洗涤2~3次后,再
(4)实验室用滴定法测定产品纯度。测定过程涉及的反应为:
2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑
Ce4++Fe2+=Ce3++Fe3+
称取2.50 g产品配成250 mL溶液,取25.00 mL置于锥形瓶中,加入V1 mLc1 mol·L-1(NH4)2Ce(NO3)6溶液,充分反应后稍作稀释,向溶液中加适量硫酸,滴加2滴邻菲罗啉指示剂,用c2 mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗标准溶液V2 mL。
①产品纯度为
②为了提高实验的精确度,该实验还需要
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


