解答题-原理综合题 适中0.65 引用1 组卷246
铁的硫化物被认为是有前景的锂电池材料,但导电性较差,放电时易膨胀。
(1) 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。
①水热法合成 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为___________ 。
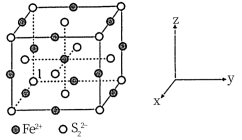
② 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为___________ (任写一个),每个 周围距离最近且相等的
周围距离最近且相等的 有
有___________ 个。
(2)①将 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
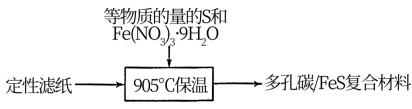
具有的优势是放电时不易膨胀且___________ 。多孔碳/ 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和___________ 。
②分别取多孔碳、多孔碳/ 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。
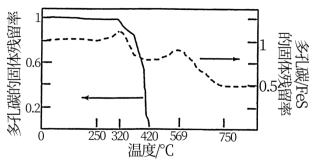
420℃~569℃时,多孔碳/ 固体残留率增大的原因是
固体残留率增大的原因是___________ 。
③ 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应:

该多孔碳/ 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子___________  。(写出计算过程)
。(写出计算过程)
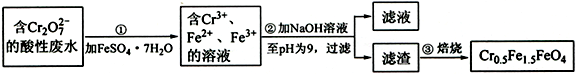
(1)
①水热法合成
②

(2)①将

②分别取多孔碳、多孔碳/

420℃~569℃时,多孔碳/
③
该多孔碳/
21-22高三上·江苏泰州·期末
类题推荐
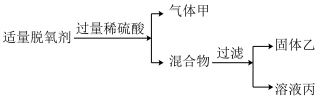
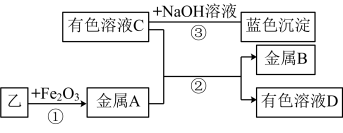
某化学兴趣小组在探究次氯酸钠溶液的性质时发现:往过量FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。请你协助他们完成该反应还原产物的探究。
(1)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为___________ 。
(2)你认为甲同学的推测是否正确?___________ (填“正确”或“不正确”)。请用简要的文字或离子方程式说明理由__________ 。根据乙同学的推测,上述反应的离子方程式为___________ 。
(3)请你设计一个实验方案,验证乙同学的推测(还原产物)是否正确。要求写出实验步骤、预期现象和结论:
(1)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为
(2)你认为甲同学的推测是否正确?
(3)请你设计一个实验方案,验证乙同学的推测(还原产物)是否正确。要求写出实验步骤、预期现象和结论:
| 实验步骤 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网