填空题 适中0.65 引用1 组卷129
按要求回答下列问题。
(1)为了防止 FeSO4 溶液变质,应在溶液中加入少量的___________ (元素符号表示)。
(2)人体血液中的下列物质不属于电解质的是___________ (填序号,下同)。
a.H2CO3 b.葡萄糖(C6H12O6) c.NaHCO3 d.NaCl
(3)区分 Na2CO3 和 NaHCO3 溶液可选用的方法或试剂是___________ 。
a.CaCl2 溶液 b.焰色试验 c.Ca(OH)2 溶液 d.NaOH 溶液
(4)下列过程必须加入氧化剂才能实现的是___________ 。
a.Cl2→ClO- b.NH3→NH c.KMnO4→MnO2 d.Fe2+→Fe3+
c.KMnO4→MnO2 d.Fe2+→Fe3+
(5)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
①用双线桥法表示电子的转移情况(只需标出电子得失和转移电子总数目)___________ 。
②上面反应中,参加氧化还原反应的硝酸占总硝酸的___________ (用百分数表示)。
(6)已知 16 g A 和 20 g B 恰好完全反应生成 0.04 mol C 和 31.76 g D,则 C 的摩尔质量为___________ 。
(1)为了防止 FeSO4 溶液变质,应在溶液中加入少量的
(2)人体血液中的下列物质不属于电解质的是
a.H2CO3 b.葡萄糖(C6H12O6) c.NaHCO3 d.NaCl
(3)区分 Na2CO3 和 NaHCO3 溶液可选用的方法或试剂是
a.CaCl2 溶液 b.焰色试验 c.Ca(OH)2 溶液 d.NaOH 溶液
(4)下列过程必须加入氧化剂才能实现的是
a.Cl2→ClO- b.NH3→NH
(5)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
①用双线桥法表示电子的转移情况(只需标出电子得失和转移电子总数目)
②上面反应中,参加氧化还原反应的硝酸占总硝酸的
(6)已知 16 g A 和 20 g B 恰好完全反应生成 0.04 mol C 和 31.76 g D,则 C 的摩尔质量为
20-21高一上·吉林长春·期末
类题推荐
I.氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示,已知这个反应速率随着溶液中c(H+)增大而加快。
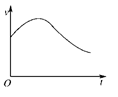
(1)反应开始时反应速率加快的原因是___________________ 。
(2)反应后期反应速率下降的原因是___________________ 。
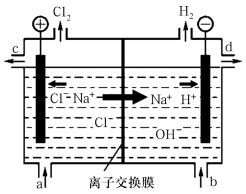
II.用惰性电极电解200 mL一定浓度的硫酸铜溶液,实验装置如图①所示,电解过程中的实验数据如图②所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。

(1)下列说法正确的是______ (填序号)。
(2)如果要使溶液恢复到电解前的状态,向溶液中加入0.8 g CuO即可,则电解后溶液的c(H+)=______ 。(3)如果向所得的溶液中加入0.1 mol Cu(OH)2后,使溶液恰好恢复到电解前的浓度和pH,电解过程中转移的电子为______ mol。
(4)如果向所得的溶液中加入0.1 mol Cu2(OH)2CO3后,使溶液恰好恢复到电解前的浓度和pH(不考虑CO2的溶解),电解过程中转移的电子为______ mol。

(1)反应开始时反应速率加快的原因是
(2)反应后期反应速率下降的原因是
II.用惰性电极电解200 mL一定浓度的硫酸铜溶液,实验装置如图①所示,电解过程中的实验数据如图②所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。

(1)下列说法正确的是
| A.电解过程中,b电极表面先有红色物质析出,后有气泡产生 |
| B.a电极上发生的反应为2H++2e-===H2↑和4OH--4e-===2H2O+O2↑ |
| C.从P点到Q点时收集到的混合气体的平均摩尔质量为12 g·mol-1 |
| D.OP段表示H2和O2混合气体的体积变化,PQ段表示O2的体积变化 |
(2)如果要使溶液恢复到电解前的状态,向溶液中加入0.8 g CuO即可,则电解后溶液的c(H+)=
(4)如果向所得的溶液中加入0.1 mol Cu2(OH)2CO3后,使溶液恰好恢复到电解前的浓度和pH(不考虑CO2的溶解),电解过程中转移的电子为
常温下,浓度均为0.1 mol·L-1的5种溶液pH如表:
请由表中数据回答:
(1)NaClO溶液显碱性的原因是___________ (用离子方程式表示)。
(2)侯氏制碱中,使NH4Cl从母液中析出的措施不包括___________ (选填编号)。
A.冷却 B.加入食盐细颗粒 C.通入CO2 D.通入NH3
(3)0.1 mol·L-1的 NaHSO3溶液中离子浓度:c(SO )
)___________ c(HSO )(填 “>”、“<”或“=”);
)(填 “>”、“<”或“=”);
要使其中的c(SO )减小,下列方法不可行的是
)减小,下列方法不可行的是___________ (选填编号)。
A.加入过量CaO(s) B.加入少量NaOH(s) C.通入过量HCl(g) D.加入少量的H2O2(aq)
(4)5种溶液中,水的电离程度最小的是(填化学式)___________ ;向氯水中加入NaHCO3可增强其漂白性,用化学平衡移动原理解释原因:___________ 。
(5)NaHSO3溶液在不同温度下均可被过量KIO3酸性溶液氧化,当NaHSO3完全消耗时有I2析出,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:___________ ;若有25.4g I2生成,则转移电子数是___________ 个。
| 溶质 | Na2CO3 | NaHCO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 10.0 | 4.0 | 10.3 |
请由表中数据回答:
(1)NaClO溶液显碱性的原因是
(2)侯氏制碱中,使NH4Cl从母液中析出的措施不包括
A.冷却 B.加入食盐细颗粒 C.通入CO2 D.通入NH3
(3)0.1 mol·L-1的 NaHSO3溶液中离子浓度:c(SO
要使其中的c(SO
A.加入过量CaO(s) B.加入少量NaOH(s) C.通入过量HCl(g) D.加入少量的H2O2(aq)
(4)5种溶液中,水的电离程度最小的是(填化学式)
(5)NaHSO3溶液在不同温度下均可被过量KIO3酸性溶液氧化,当NaHSO3完全消耗时有I2析出,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网