单选题 适中0.65 引用4 组卷341
已知A(s) +B(g) 2C(g) ΔH<0,体系中C的物质的量分数与温度的关系如下图所示。
2C(g) ΔH<0,体系中C的物质的量分数与温度的关系如下图所示。
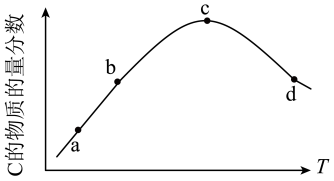
下列说法正确的是

下列说法正确的是
| A.其它条件不变时,增大压强平衡不移动 |
| B.该反应的平衡常数表达式K= |
| C.上述图象中,b点已达到化学平衡状态 |
| D.化学平衡常数K(c)<K(d) |
20-21高二上·北京·期末
类题推荐
已知浓度商(Qc)表示任意状态下反应体系中物质的浓度关系,其表达式与化学平衡常数的表达式相同。保持温度和体积不变,可逆反应:A(s) + 2B(g) 2C(g) + D(g) △H<0, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是
2C(g) + D(g) △H<0, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是
 2C(g) + D(g) △H<0, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是
2C(g) + D(g) △H<0, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是| 容器 | 体积 | 起始物质 | 平衡时C的 物质的量 | 平衡时B的 体积分数 | 平衡常数 |
| 甲 | 1L | 1molA+2molB | 1mol | φ甲 | K甲 |
| 乙 | 1L | 4molC+2molD | n1 mol | φ乙 | K乙 |
| 丙 | 2L | 4molC+2molD | n2 mol | φ丙 | K丙 |
| A.在建立平衡的过程中,甲的Qc逐渐减小,乙和丙的Qc逐渐增大 |
| B.K甲=K丙>K乙 |
| C.升高甲的温度,可使φ甲=φ乙 |
| D.n1=1.6,n2=2 |
某温度下,某反应达平衡时平衡常数K=c(C)·c(D)/c(A)·c(B)。恒容时,温度升高,C的物质的量浓度减小。下列说法正确的是( )
| A.该反应的焓变ΔH>0 |
| B.恒温恒容时,增大体系压强,c(D)一定增大 |
| C.升高温度,逆反应速率减小 |
D.该反应的化学方程式可能为A(g)+B(g) C(g)+D(g) C(g)+D(g) |
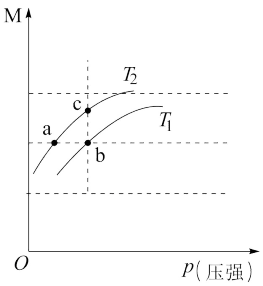
常压下羰基化法精炼镍的原理为: Ni(CO)4(g) Ni (s) +4CO(g) ΔH >0,在平衡体系中,气体的平均摩尔质量M (
Ni (s) +4CO(g) ΔH >0,在平衡体系中,气体的平均摩尔质量M ( )在不同温度下随压强的变化曲线如图所示。下列说法正确的
)在不同温度下随压强的变化曲线如图所示。下列说法正确的

| A.该反应达到平衡时, v分解[Ni(CO)4]=4v消耗(CO) |
| B.vb(正)> va(逆) |
| C.K(a)=K(c)>K(b) |
| D.当M=100g·mol-1时, n(Ni(CO)4):n(CO)=1: 1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


