单选题 适中0.65 引用2 组卷454
H2A为二元弱酸,常温下,将NaOH溶液加入到H2A溶液中,在不同pH环境下,不同形态的粒子(H2A、HA-、A2-)的分布分数如图所示。下列说法正确的是


| A.曲线Ⅰ代表H2A,H2A一级电离常数的数量级为 |
| B.氢离子浓度相同时,溶液中 |
| C.NaHA溶液中,促进水电离的趋势大于抑制趋势 |
| D.1L0.1mol/LNa2A溶液中,n(HA-)+2n(A2-)+n(H2A)=0.1mol |
2021·河北·模拟预测
类题推荐
H2A为二元酸,其电离过程为:H2A H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
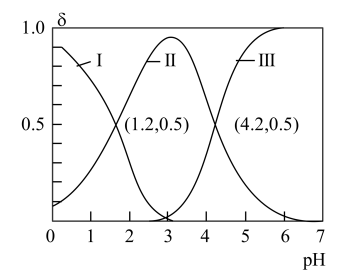
| A.H2A的Kal的数量级为10-1 |
| B.当溶液中c(H2A)=c(A2-)时,pH=2.7 |
| C.曲线Ⅱ表示A2- |
| D.向pH=4.2的溶液中继续滴加NaOH溶液,水的电离程度持续变大 |
常温下,向0.1mol∙L-1二元弱酸H2A溶液中逐滴加入NaOH溶液,H2A、HA-、A2-的物质的量分数[已知 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是
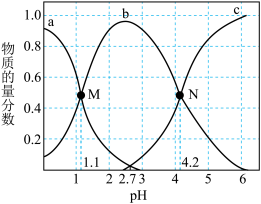

| A.b曲线代表A2-的物质的量分数随pH的变化 |
| B.M点pH=1.1时,溶液中微粒浓度的大小关系为:c(H+)>c(HA-)=c(H2A)>c(OH-) |
| C. pH=2.73时,c(A2-)+c(HA-)+ c(H2A)=0.1mol∙L-1 |
| D.N点pH=4.2时,c(A2-)=c(HA-),溶液中不存在H2A分子 |
H2A为二元酸,其电离过程为: 、
、 。常温时,向10mL0.1mol/LH2A溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(
。常温时,向10mL0.1mol/LH2A溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数( )随pH变化的关系如图所示。下列说法正确的是
)随pH变化的关系如图所示。下列说法正确的是
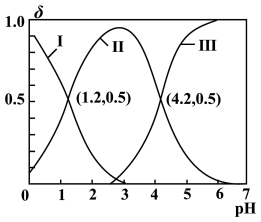

| A.H2A的Ka1的数量级为10-1 |
| B.当溶液中 |
| C.0.01mol/LNaHA溶液中: |
| D.向pH=4.2的溶液中继续滴加NaOH溶液,水的电离程度持续变大 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


