单选题 适中0.65 引用1 组卷256
电解法制取Na2FeO4同时获得H2,工作原理如图所示。下列说法错误的是
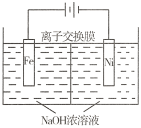

| A.铁电极作阳极,电极反应式为Fe-6e-+8OH-= |
| B.离子交换膜为阳离子交换膜 |
| C.电解一段时间后,阳极区NaOH浓度降低 |
| D.由于Na2FeO4具有强氧化性,电解过程中,须将阴极产生的气体及时排出 |
20-21高三上·山东·阶段练习
类题推荐
电解法制取有广泛用途的Na2FeO4,同时获得氢气。工作原理如图1所示,c( Na2FeO4)随初始c(NaOH)的变化如图2。

已知:FeO42-为紫红色;Na2FeO4只在强碱性条件下稳定,易被H2还原;溶液中OH-浓度过高,铁电极区会产生红褐色物质。下列说法错误的是

已知:FeO42-为紫红色;Na2FeO4只在强碱性条件下稳定,易被H2还原;溶液中OH-浓度过高,铁电极区会产生红褐色物质。下列说法错误的是
| A.制备Na2FeO4的电极反应为Fe-6e-+8OH-=FeO42-+4H2O |
| B.电解过程中,须将阴极产生的气体及时排出 |
| C.MN两点中c(Na2FeO4)低于最高值的原因不同,在M点会有Fe(OH)3生成 |
| D.图1中的离子交换膜为阴离子交换膜,电解过程中,阴极区附近pH会增大 |
已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。工业上用电解法制取有广泛用途的Na2FeO4, 同时获得氢气。工作原理如图所示。下列说法正确的是

| A.m接电源的负极 |
| B.电解一段时间后,阳极区的c(OH-)增大 |
| C.电极Ni为阳极,电极反应为2H2O+2e-=H2↑+20H- |
| D.为防止Na2FeO4与H2反应,电解过程中须将阴极产生的气体及时排出 |
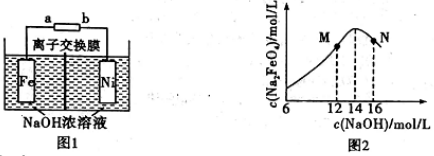
用电解法可制取有广泛用途的Na2FeO4:Fe+2H2O+ 2NaOH Na2FeO4+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeOH42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。下列说法不正确的是
Na2FeO4+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeOH42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。下列说法不正确的是
 Na2FeO4+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeOH42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。下列说法不正确的是
Na2FeO4+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeOH42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。下列说法不正确的是
| A.a是电源的正极 |
| B.电解一段时间后,c(OH-)降低的区域在阴极室 |
| C.电解过程中,阳极发生的电极方程式为Fe+8OH--6e-==FeO42-+4H2O |
| D.如图2,N点c(Na2FeO4)低于最高值的原因是氢氧化钠溶液浓度过高 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


