解答题-原理综合题 适中0.65 引用1 组卷129
绿色发展、生态保护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少氮氧化物在大气中的排放是环境保护的重要内容之一、请回答下列问题:
(1)研究氮氧化物与悬浮大气中海盐粒子的相互作用时,涉及如下反应:
Ⅰ.2NO2(g)+NaCl(s)⇌ NaNO3(s)+ClNO(g) K1 ΔH1
Ⅱ.2NO(g)+Cl2(g)⇌2ClNO(g) K2 ΔH2
则4NO2(g)+2NaCl(s)⇌ 2NaNO3(s)+2NO(g)+Cl2(g) ΔH=___________ (用ΔH1、ΔH2表示);平衡常数K=___________ (用K1、K2表示)
(2)N2O5在一定条件下可发生分解反应:2N2O5(g)⇌ 4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如表所示:
①反应开始时体系压强为p0,第2 min时体系压强为p1,则p1 :p0=___________ 。2~5 min内用NO2表示的该反应的平均反应速度为___________ 。
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是___________ (填标号)。
a.NO2和O2的浓度比保持不变 b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5) d.气体的密度保持不变
(3)汽车排气管装有的三元催化装置,可以消除CO、NO等的污染,反应机理如下:
Ⅰ:NO+Pt(s)=NO(*) [Pt(s)表示催化剂,NO(*)表示吸附态NO,下同]
Ⅱ:CO+Pt(s)=CO(*)
Ⅲ:NO(*)=N(*)+O(*)
Ⅳ:CO(*)+O(*)=CO2+2Pt(s)
Ⅴ:N(*)+N(*)=N2+2Pt(s)
Ⅵ:NO(*)+N(*)=N2O+2Pt(s)
尾气中反应物及生成物浓度随温度的变化关系如图。
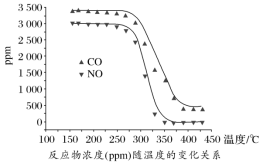
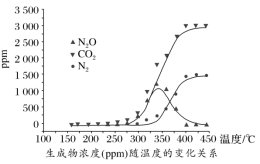
①330 ℃以下的低温区发生的主要反应的化学方程式是___________ 。
②反应V的活化能___________ 反应Ⅵ的活化能(填“<”、“>”或“=”),理由是:___________ 。
(1)研究氮氧化物与悬浮大气中海盐粒子的相互作用时,涉及如下反应:
Ⅰ.2NO2(g)+NaCl(s)⇌ NaNO3(s)+ClNO(g) K1 ΔH1
Ⅱ.2NO(g)+Cl2(g)⇌2ClNO(g) K2 ΔH2
则4NO2(g)+2NaCl(s)⇌ 2NaNO3(s)+2NO(g)+Cl2(g) ΔH=
(2)N2O5在一定条件下可发生分解反应:2N2O5(g)⇌ 4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如表所示:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c(N2O5)/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
①反应开始时体系压强为p0,第2 min时体系压强为p1,则p1 :p0=
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是
a.NO2和O2的浓度比保持不变 b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5) d.气体的密度保持不变
(3)汽车排气管装有的三元催化装置,可以消除CO、NO等的污染,反应机理如下:
Ⅰ:NO+Pt(s)=NO(*) [Pt(s)表示催化剂,NO(*)表示吸附态NO,下同]
Ⅱ:CO+Pt(s)=CO(*)
Ⅲ:NO(*)=N(*)+O(*)
Ⅳ:CO(*)+O(*)=CO2+2Pt(s)
Ⅴ:N(*)+N(*)=N2+2Pt(s)
Ⅵ:NO(*)+N(*)=N2O+2Pt(s)
尾气中反应物及生成物浓度随温度的变化关系如图。


①330 ℃以下的低温区发生的主要反应的化学方程式是
②反应V的活化能
21-22高三上·福建·阶段练习
类题推荐
“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一、请回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g) ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH3=-221 kJ·mol-1
若某反应的平衡常数表达式为K= ,则此反应的热化学方程式为
,则此反应的热化学方程式为_______ 。
(2)N2O5在一定条件下可发生分解反应:2N2O5(g) ⇌4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如表:
①反应开始时体系压强为p0,第2 min时体系压强为p1,则p1∶p0=_______ 。2~5 min内用NO2表示的该反应的平均反应速率为_______ 。
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是_______ (填字母)。
a.NO2和O2的浓度比保持不变 b.容器中压强不再变化
c.2 正(NO2)=
正(NO2)= 逆(N2O5) d.气体的密度保持不变
逆(N2O5) d.气体的密度保持不变
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g) ⇌NO(g)+CO2(g),该反应中正反应速率 正=k正·p(NO2)·p(CO),逆反应速率
正=k正·p(NO2)·p(CO),逆反应速率 逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为
逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为_______ (用k正、k逆表示)。
(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200℃、400℃、600℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。
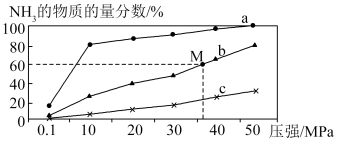
曲线a对应的温度是_______ 。
(1)已知:N2(g)+O2(g)=2NO(g) ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH3=-221 kJ·mol-1
若某反应的平衡常数表达式为K=
(2)N2O5在一定条件下可发生分解反应:2N2O5(g) ⇌4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如表:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c(N2O5)/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
①反应开始时体系压强为p0,第2 min时体系压强为p1,则p1∶p0=
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是
a.NO2和O2的浓度比保持不变 b.容器中压强不再变化
c.2
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g) ⇌NO(g)+CO2(g),该反应中正反应速率
(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200℃、400℃、600℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。

曲线a对应的温度是
“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。请回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g) ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH3=-221 kJ·mol-1
若某反应的平衡常数表达式为K= ,则此反应的热化学方程式为
,则此反应的热化学方程式为____________________ 。
(2)N2O5在一定条件下可发生分解反应:2N2O5(g) 4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
①反应开始时体系压强为p0,第2 min时体系压强为p1,则p1∶p0=________ 。2~5 min内用NO2表示的该反应的平均反应速率为________________ 。
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是________________ (填字母)。
a.NO2和O2的浓度比保持不变
b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5)
d.气体的密度保持不变
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g) NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为
NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为________________ (用k正、k逆表示)。
(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。
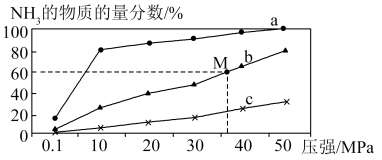
①曲线a对应的温度是________ 。
②M点对应的H2的转化率是________ 。
(1)已知:N2(g)+O2(g)=2NO(g) ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH3=-221 kJ·mol-1
若某反应的平衡常数表达式为K=
(2)N2O5在一定条件下可发生分解反应:2N2O5(g)
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c(N2O5)/ (mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是
a.NO2和O2的浓度比保持不变
b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5)
d.气体的密度保持不变
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g)
(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。

①曲线a对应的温度是
②M点对应的H2的转化率是
“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。请回答下列问题:
(1)已知:N2(g)+O2(g)===2NO(g) ΔH1= +180.5 kJ/mol
C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
2C(s)+O2(g)===2CO(g) ΔH3=-221 kJ/mol
若某反应的平衡常数表达式为K=[c(N2)·c2(CO2)]/[c2(NO)·c2(CO)],则此反应的热化学方程式为:_____________ 。
(2)N2O5在一定条件下可发生分解:2N2O5(g) 4NO2(g)+O2(g),某温度下恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
4NO2(g)+O2(g),某温度下恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
①反应开始时体系压强为p0,第2 min时体系压强为p1,则p1∶p0=________ 。2~5 min内用NO2表示的该反应的平均反应速率为________ 。
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是________ (填字母)。
a.NO2和O2的浓度比保持不变 b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5) d.气体的密度保持不变
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g) NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为
NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为________ (用k正、k逆表示)。
(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。

①曲线a对应的温度是________ 。
②M点对应的H2的转化率是________ 。
(5)常温下,联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的电离平衡常数值_______________ 。(已知:N2H4+H+ N2H5+的K=8.7×107 Kw=1.0×10-14)
N2H5+的K=8.7×107 Kw=1.0×10-14)
(1)已知:N2(g)+O2(g)===2NO(g) ΔH1= +180.5 kJ/mol
C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
2C(s)+O2(g)===2CO(g) ΔH3=-221 kJ/mol
若某反应的平衡常数表达式为K=[c(N2)·c2(CO2)]/[c2(NO)·c2(CO)],则此反应的热化学方程式为:
(2)N2O5在一定条件下可发生分解:2N2O5(g)
 4NO2(g)+O2(g),某温度下恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
4NO2(g)+O2(g),某温度下恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c(N2O5)/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是
a.NO2和O2的浓度比保持不变 b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5) d.气体的密度保持不变
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g)
 NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为
NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。

①曲线a对应的温度是
②M点对应的H2的转化率是
(5)常温下,联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的电离平衡常数值
 N2H5+的K=8.7×107 Kw=1.0×10-14)
N2H5+的K=8.7×107 Kw=1.0×10-14) 组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


