解答题-工业流程题 适中0.65 引用1 组卷43
碱式硫酸铁[Fe(OH)SO4]是黄褐色固体,常用作媒染剂和净水剂。一种利用废铁屑(含少量Al、Al2O3、Fe2O3 等杂质)生产碱式硫酸铁的工艺流程如图所示:
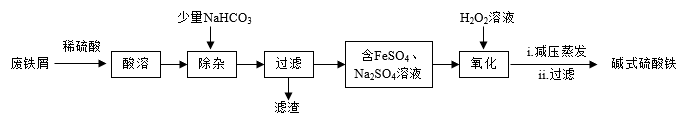
已知:①部分金属阳离子生成氢氧化物沉淀时溶液的pH如表:
②Fe(OH)2+发生电离:Fe(OH)2+ Fe3++OH-。
Fe3++OH-。
请回答下列问题:
(1)加入少量NaHCO3,调节pH的范围是___________ 。
(2)“氧化”过程中,发生反应的离子方程式为___________ ;该过程某同学选用稀硝酸代替H2O2溶液完成反应,你认为不足之处是___________ 。
(3)“氧化”过程中,若硫酸加入量过小,容易生成___________ (填化学式)沉淀;若硫酸加入量过大,不利于产品形成,试从平衡移动的角度分析原因是___________ 。
(4)将所得产品加蒸馏水溶解,为检验是否含有Fe2+,最好选用的试剂是___________ (填字母代号)。
A.氯水 B.KSCN溶液 C.K3[Fe(CN)6]溶液 D.H2O2溶液

已知:①部分金属阳离子生成氢氧化物沉淀时溶液的pH如表:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀 | 7.5 | 2.3 | 3.4 |
| 沉淀完全 | 9.7 | 3.2 | 4.4 |
②Fe(OH)2+发生电离:Fe(OH)2+
请回答下列问题:
(1)加入少量NaHCO3,调节pH的范围是
(2)“氧化”过程中,发生反应的离子方程式为
(3)“氧化”过程中,若硫酸加入量过小,容易生成
(4)将所得产品加蒸馏水溶解,为检验是否含有Fe2+,最好选用的试剂是
A.氯水 B.KSCN溶液 C.K3[Fe(CN)6]溶液 D.H2O2溶液
20-21高二上·重庆渝中·阶段练习
类题推荐
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)加入少量NaHCO3的目的是________________ ,该工艺中“搅拌”的作用是___________ 。
(2)反应Ⅱ中的离子方程式为____________ ,在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2的作用是_______________ 。(用化学方程式表示)
(3)生产中碱式硫酸铁溶液蒸发时需要在减压条件下的原因是____________ 。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为__________ 。(填写字母)
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入少量NaHCO3的目的是
(2)反应Ⅱ中的离子方程式为
(3)生产中碱式硫酸铁溶液蒸发时需要在减压条件下的原因是
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:
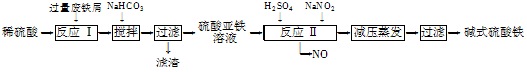
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
回答下列问题:
(1)反应Ⅰ中发生的氧化还原反应的化学方程式为______ 。
(2)加入少量NaHCO3的目的是调节pH,使溶液中的______ (填“Fe3+”、“Fe2+”或“Al3+”)沉淀。该工艺流程中“搅拌”的作用是______ 。
(3)反应Ⅱ的离子方程式为______ 。在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作______ 。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为______ 。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为______ 。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为______ (填字母)。
A. 氯水 B. KSCN溶液 C. NaOH溶液 D. 酸性KMnO4溶液

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)反应Ⅰ中发生的氧化还原反应的化学方程式为
(2)加入少量NaHCO3的目的是调节pH,使溶液中的
(3)反应Ⅱ的离子方程式为
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为
A. 氯水 B. KSCN溶液 C. NaOH溶液 D. 酸性KMnO4溶液
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]工艺流程如下:
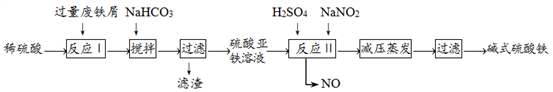
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
回答下列问题:
(1)反应I溶液中存在的金属阳离子有___________________________ 。
(2)加入少量NaHCO3的目的是调节pH,使溶液中的________ (填“Fe3+”、“Fe2+”或“Al3+”)沉淀。该工艺流程中“搅拌”的作用是______________________ 。
(3)反应Ⅱ的离子方程式为____________________________ 。在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作______________ 。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为________ 。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42-聚合离子。该水解反应的离子方程式为____________________________ 。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为________ (填字母)。
A. 氯水 B. KSCN溶液 C. NaOH溶液 D. 酸性KMnO4溶液

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)反应I溶液中存在的金属阳离子有
(2)加入少量NaHCO3的目的是调节pH,使溶液中的
(3)反应Ⅱ的离子方程式为
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42-聚合离子。该水解反应的离子方程式为
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为
A. 氯水 B. KSCN溶液 C. NaOH溶液 D. 酸性KMnO4溶液
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


