解答题-实验探究题 适中0.65 引用2 组卷178
叠氮化钠(NaN3)可用作医药原料,由叠氮化钠可制备四唑类化合物,从而进一步合成抗生素头孢菌素药物。
查阅资料:
①水合肼(N2H4●H2O)有毒且不稳定,具有强还原性和强碱性。
②有关物质的物理性质如表:
回答下列问题:
(1)由叠氮化钠制备四唑类化合物。
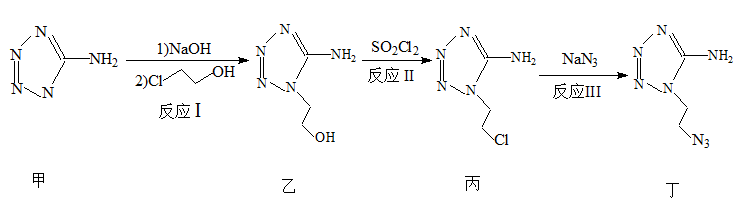
①反应I的反应类型是____ 。甲、乙、丙、丁四种化合物中,氮元素的质量分数最大的是___ 。
②SO2Cl2与水反应生成两种强酸,SO2Cl2与水反应的化学方程式为___________ .
(2)合成水合肼。
NaClO碱性溶液与尿素[CO(NH2)2]水溶液在40°C以下反应一段时间后,再迅速升温至110°C继续反应可以制得水合肼,同时有碳酸钠生成。实验室合成水合胖的装置如图所示。
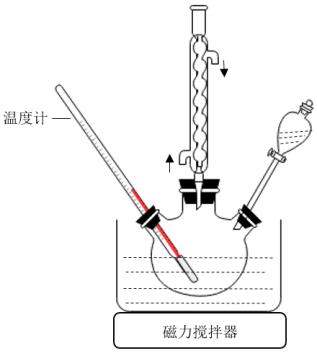
①制取N2H4●H2O的离子方程式为_______________
②实验中通过分液漏斗滴加的溶液是__________ ,理由是________________ 。
(3)水合肼法制备叠氮化钠。
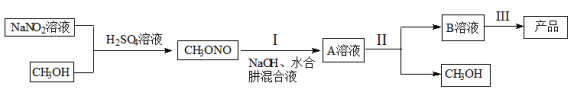
①实验室模拟工艺流程步骤I制备叠氮化钠的反应原理为N2H4●H2O(aq) +CH3ONO(g) +NaOH(aq)=NaN3(ag)+CH3OH(aq)+3H2O(l) △H<0。研究表明该反应在20°C左右反应的选择性和转化率最高。实验时可以采取的措施是______ (写一种)。
②步骤II回收CH3OH的实验操作名称为__________
查阅资料:
①水合肼(N2H4●H2O)有毒且不稳定,具有强还原性和强碱性。
②有关物质的物理性质如表:
物质 | 熔点/C | 沸点/C | 溶解性 |
| CH3OH | -97 | 64.7 | 与水互溶 |
| 水台肼(N2H4∙H2O) | - 40 | 118.5 | 与水、醇互溶,不溶于乙醚 |
| 亚硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇,乙醚 |
| 叠氮化钠(NaN3) | 275(410易分解) | - | 易溶于水,微溶于醇,不溶于乙醚 |
(1)由叠氮化钠制备四唑类化合物。

①反应I的反应类型是
②SO2Cl2与水反应生成两种强酸,SO2Cl2与水反应的化学方程式为
(2)合成水合肼。
NaClO碱性溶液与尿素[CO(NH2)2]水溶液在40°C以下反应一段时间后,再迅速升温至110°C继续反应可以制得水合肼,同时有碳酸钠生成。实验室合成水合胖的装置如图所示。

①制取N2H4●H2O的离子方程式为
②实验中通过分液漏斗滴加的溶液是
(3)水合肼法制备叠氮化钠。

①实验室模拟工艺流程步骤I制备叠氮化钠的反应原理为N2H4●H2O(aq) +CH3ONO(g) +NaOH(aq)=NaN3(ag)+CH3OH(aq)+3H2O(l) △H<0。研究表明该反应在20°C左右反应的选择性和转化率最高。实验时可以采取的措施是
②步骤II回收CH3OH的实验操作名称为
20-21高三上·安徽·阶段练习
类题推荐
叠氮化钠(NaN3)是汽车安全气囊最理想的气体发生剂原料。下面是工业水合肼法制备叠氮化钠的工艺流程:

查阅资料:
①水合肼(N2H4·H2O)有毒且不稳定,具有强还原性和强碱性。
②有关物质的物理性质如下表:
(1)合成水合肼。
实验室合成水合肼装置如图所示。NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。

①制取N2H4·H2O的离子方程式为_________ 。
②实验中通过分液漏斗滴加的溶液是_________ ,理由是_________ 。
(2)水合肼法制备叠氮化钠。
①实验室模拟工艺流程步骤Ⅰ制备叠氮化钠的反应原理为:N2H4·H2O(aq)+CH3ONO(g)+NaOH(aq)=NaN3(aq)+CH3OH(aq)+3H2O(l) △H﹤0, 研究表明该反应在20℃左右反应的选择性和转化率最高,实验时可以采取的措施是_________ 。
②步骤Ⅱ回收CH3OH的实验操作名称为________ 。
③请设计由B溶液获得叠氮化钠(NaN3)产品的实验方案:_________ [实验中可供选择的试剂有:乙醇、乙醚;除常用仪器外须使用的仪器有:布氏漏斗、真空干燥箱]。

查阅资料:
①水合肼(N2H4·H2O)有毒且不稳定,具有强还原性和强碱性。
②有关物质的物理性质如下表:
| 物质 | 熔点℃ | 沸点℃ | 溶解性 |
| CH3OH | -97 | 64.7 | 与水互溶 |
| 水合肼(N2H4·H2O) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚 |
| 亚硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇、乙醚 |
| 叠氮化钠(NaN3) | 275 (410易分解) | —— | 易溶于水,微溶于醇, 不溶于乙醚 |
实验室合成水合肼装置如图所示。NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。

①制取N2H4·H2O的离子方程式为
②实验中通过分液漏斗滴加的溶液是
(2)水合肼法制备叠氮化钠。
①实验室模拟工艺流程步骤Ⅰ制备叠氮化钠的反应原理为:N2H4·H2O(aq)+CH3ONO(g)+NaOH(aq)=NaN3(aq)+CH3OH(aq)+3H2O(l) △H﹤0, 研究表明该反应在20℃左右反应的选择性和转化率最高,实验时可以采取的措施是
②步骤Ⅱ回收CH3OH的实验操作名称为
③请设计由B溶液获得叠氮化钠(NaN3)产品的实验方案:
叠氮化钠(NaN3)是汽车安全气囊的气体发生剂的成分。工业上可用水合肼(N2H4·H2O)法制备叠氮化钠,工艺流程如图所示:
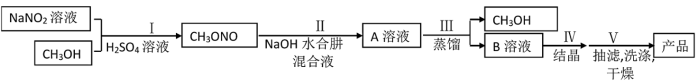
相关物质的物理性质如表:
(1)水合肼的合成
水合肼有毒,有较强还原性100℃以上易分解失水。实验室用NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后, 再迅速升温至110℃继续反应制得水合肼制取N2H4·H2O的离子方程式为_______ 。
(2)水合肼法制备叠氮化钠(NaN3)。
实验室模拟工艺流程步骤II制备叠氮化钠的反应原理为:N2H4·H2O(aq)+CH3ONO(g)+NaOH(aq)=NaN3(aq)+CH3OH(aq)+3H2O(l) ΔH<0.装置如图:
①图中X处连接的最合适装置应为图中的_______ 。
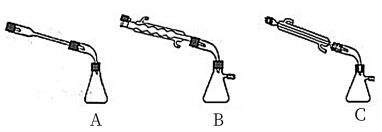
②步骤II中制备叠氮化钠的操作是_______ (填序号);步骤III中对A溶液进行蒸馏的合理操作顺序是________ 。(填序号)
(A)开K1、K2,关闭K3 (B)打开K3 (C)加热 (D)关闭K1、K2
③步骤IV对溶液B加热蒸发至原溶液体积的1/3,NaN3结晶析出。步骤V用到的抽滤装置,主要由_______ 和_______ 组成,洗涤晶体的洗涤剂应选用 _______ 。洗涤的具体操作是:_______ 。

相关物质的物理性质如表:
| 物质 | 熔点℃ | 沸点℃ | 溶解性 |
| CH3OH | -97 | 64.7 | 与水互溶 |
| 水合肼(N2H4·H2O) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚 |
| 肼(N2H4) | 1.4 | 113.5 | 与水、醇互溶,不溶于乙醚 |
| 亚硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇、乙醚 |
| 叠氮化钠(NaN3) | 275(410易分解) | _______ | 易溶于水,微溶于醇,不溶于乙醚 |
水合肼有毒,有较强还原性100℃以上易分解失水。实验室用NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后, 再迅速升温至110℃继续反应制得水合肼制取N2H4·H2O的离子方程式为
(2)水合肼法制备叠氮化钠(NaN3)。
实验室模拟工艺流程步骤II制备叠氮化钠的反应原理为:N2H4·H2O(aq)+CH3ONO(g)+NaOH(aq)=NaN3(aq)+CH3OH(aq)+3H2O(l) ΔH<0.装置如图:

①图中X处连接的最合适装置应为图中的

②步骤II中制备叠氮化钠的操作是
(A)开K1、K2,关闭K3 (B)打开K3 (C)加热 (D)关闭K1、K2
③步骤IV对溶液B加热蒸发至原溶液体积的1/3,NaN3结晶析出。步骤V用到的抽滤装置,主要由
水合肼(N2H4•H2O)是制备叠氮化钠(NaN3)的原料,而叠氮化钠又是汽车安全气囊最理想的气体发生剂的原料。如图是工业水合肼法制备叠氮化钠的工艺流程。

查阅资料:①水合肼有毒且不稳定,具有强还原性和强碱性;
②有关物质的物理性质如下表:
物质 | 甲醇 | 水合肼 | 亚硝酸甲酯 | 叠氮化钠 |
熔点(℃) | -97 | -40 | -17 | 275(410℃:易分解) |
沸点(℃) | 64.7 | 118.5 | -12 | — |
回答下列问题:
Ⅰ.合成水合肼。实验室水合肼合成水合肼装置如图所示,NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
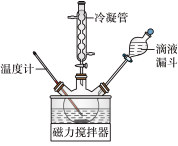
(1)实验中通过滴液漏斗向三颈瓶中缓慢滴加NaClO溶液的原因是
II.制备叠氮化钠。实验室可利用如图所示的装置及药品制备叠氮化钠。
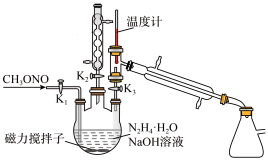
(2)①根据实验发现温度在20℃左右反应的转化率最高,但是该反应属于放热反应,因此可采取的措施是
②写出该方法制备叠氮化钠的化学方程式:
(3)流程中由B溶液获得叠氮化钠产品的实验步骤为
(4)化工生产中,多余的叠氮化钠常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。若处理6.5gNaN3,理论上需加入0.5mol • L-1的NaClO溶液
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


