解答题-工业流程题 适中0.65 引用2 组卷275
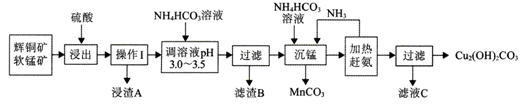
辉铜矿的主要成分是Cu2S,含较多的Fe2O3、SiO2杂质:软锰矿的主要成分是MnO2,含有较多的SiO2杂质。辉铜矿的湿法冶炼,目前国内外都处于探索之中。自氧化还原氨分离法是一种较为理想的湿法冶炼方法,工艺流程如图:
回答下列问题:
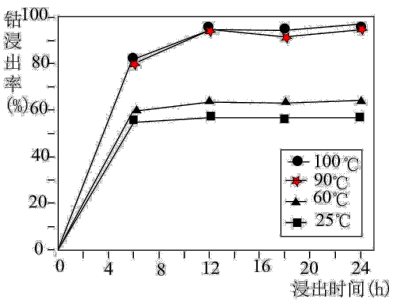
(1)将100g辉铜矿和40g98%的浓硫酸混合,在80~90℃条件下浸出2.5h,铜的浸出率随软锰矿用量的变化如表:
则浸出100g辉铜矿,软锰矿的最适宜用量为___________ g。
(2)“浸出”后的浸出液中含有CuSO4、MnSO4、Fe2(SO4)3等溶质,“滤渣I”中含有淡黄色固体单质,则“浸出”时产生淡黄色固体的化学方程式为___________ 。
(3)研究表明矿物中Fe2O3在“浸出”反应中起着重要的媒介作用,促进Cu2S与MnO2的溶解,其反应过程如下:
①Fe2O3+3H2SO4=Fe2(SO4) 3+3H2O;
②Cu2S+2Fe2(SO4)3=2CuSO2+4FeSO4+S↓
③___________ 。(写出反应的化学方程式)
(4)“滤渣II”的主要成分是___________ ;“沉锰”后,得到的深蓝色溶液中除NH 、H+外,还含有的阳离子为
、H+外,还含有的阳离子为___________ 。(写化学式)
(5)“滤液III”经结晶可得到(NH4)2SO4晶体。结晶时,当___________ 时,即可停止加热。
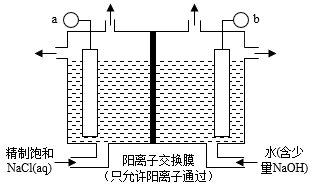
(6)如图表示用石墨作电极,在一定条件下电解饱和食盐水制取Cl2时,与a相连的电极上会产生少量的ClO2,产生ClO2电极反应式:___________ ;与b相连的电极上的电极反应式:___________ ;电解一段时间,当阴极产生标准状况下气体112mL时,停止电解,则通过阳离子交换膜的阳离子物质的量为___________ mol。

回答下列问题:
(1)将100g辉铜矿和40g98%的浓硫酸混合,在80~90℃条件下浸出2.5h,铜的浸出率随软锰矿用量的变化如表:
| 锰矿用量(g) | 15 | 20 | 25 | 30 | 35 |
| 铜浸出率(%) | 84.0 | 86.5 | 89.8 | 89.9 | 89.9 |
则浸出100g辉铜矿,软锰矿的最适宜用量为
(2)“浸出”后的浸出液中含有CuSO4、MnSO4、Fe2(SO4)3等溶质,“滤渣I”中含有淡黄色固体单质,则“浸出”时产生淡黄色固体的化学方程式为
(3)研究表明矿物中Fe2O3在“浸出”反应中起着重要的媒介作用,促进Cu2S与MnO2的溶解,其反应过程如下:
①Fe2O3+3H2SO4=Fe2(SO4) 3+3H2O;
②Cu2S+2Fe2(SO4)3=2CuSO2+4FeSO4+S↓
③
(4)“滤渣II”的主要成分是
(5)“滤液III”经结晶可得到(NH4)2SO4晶体。结晶时,当
(6)如图表示用石墨作电极,在一定条件下电解饱和食盐水制取Cl2时,与a相连的电极上会产生少量的ClO2,产生ClO2电极反应式:

20-21高三上·河北石家庄·期中
类题推荐
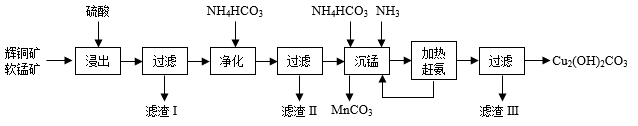
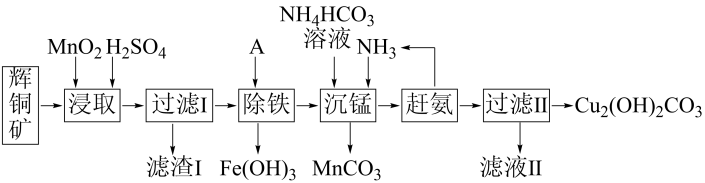
铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
已知:常温下几种离子沉淀时的pH如下表(当离子浓度≤1.0×10-5mol·L-1时完全沉淀)
(1)下列措施不能加快浸取速率的是___________。(填字母)
(2)滤渣I的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:___________ 。
(3)研究表明矿物中Fe2O3在“浸取”反应中起着重要的媒介作用,促进Cu2S与MnO2的溶解,其反应过程如下:
①Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
②Cu2S+2Fe2(SO4)3=2CuSO4+4FeSO4+S↓
③___________ (写出反应的化学方程式)。
Fe2O3可明显加快“浸取”的速率,可能的原因是___________ 。
(4)①常温“除铁”的方法是通过加入试剂A调节溶液的pH,使Fe3+转化为Fe(OH)3,则试剂A最好是___________ 。
A.氨水 B.Cu C.CuO D.CuCl2
②“除铁”时调节溶液pH的适宜范围为___________ ,Fe(OH)3的Ksp为___________ 。
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为___________ 。
(6)从滤液Ⅱ获得(NH4)2SO4晶体,当观察到___________ 现象时,即可停止加热。

已知:常温下几种离子沉淀时的pH如下表(当离子浓度≤1.0×10-5mol·L-1时完全沉淀)
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀pH | 7.5 | 2.0 | 4.7 | 8.3 |
| 完全沉淀pH | 9.0 | 3.0 | 6.7 | 9.8 |
(1)下列措施不能加快浸取速率的是___________。(填字母)
| A.将辉铜矿粉碎 | B.延长浸取时间 | C.充分搅拌 | D.适当增大硫酸浓度 |
(3)研究表明矿物中Fe2O3在“浸取”反应中起着重要的媒介作用,促进Cu2S与MnO2的溶解,其反应过程如下:
①Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
②Cu2S+2Fe2(SO4)3=2CuSO4+4FeSO4+S↓
③
Fe2O3可明显加快“浸取”的速率,可能的原因是
(4)①常温“除铁”的方法是通过加入试剂A调节溶液的pH,使Fe3+转化为Fe(OH)3,则试剂A最好是
A.氨水 B.Cu C.CuO D.CuCl2
②“除铁”时调节溶液pH的适宜范围为
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为
(6)从滤液Ⅱ获得(NH4)2SO4晶体,当观察到
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网