解答题-原理综合题 适中0.65 引用1 组卷34
根据《化学反应原理》知识,按要求作答。
I.在一定条件下,以CH4和H2O为原料,通过下列反应制备甲醇(CH3OH)。
已知:①CH4+H2O(g) CO(g)+3H2(g)△H=+206.0kJ·mol-1
CO(g)+3H2(g)△H=+206.0kJ·mol-1
②CO(g)+2H2(g) CH3OH(g)△H=-129.0kJ·mol-1
CH3OH(g)△H=-129.0kJ·mol-1
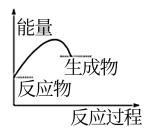
(1)反应②的正反应属于___ (填“吸热”或“放热”)反应。
(2)上述两个反应达到平衡后,在其它条件不变的情况下,通过减小容器体积增大压强,则化学平衡向逆反应方向移动的是___ (填“①”或“②”)。
(3)在密闭容器中发生①反应,若CH4起始浓度为2.0mol·L-1,水蒸气起始浓度为3.0mol·L-1,反应进行5min后,测得CH4浓度为0.5mol·L-1,则v(CH4)=___ mol·L-1·min-1。
Ⅱ.常温下,浓度均为0.1mol·L-1的两种溶液;①氨水②NH4Cl溶液。
(4)写出①氨水中NH3·H2O的电离方程式:___ 。
(5)测得②溶液的pH<7,则溶液中c(NH )
)___ c(Cl-)(填“>”“<”或“=”),写出②溶液发生水解反应的离子方程式:___ 。
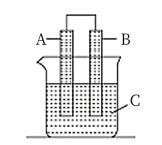
Ⅲ.如图所示装置,用惰性电极电解熔融氯化钠(2NaCl 2Na+Cl2↑)。
2Na+Cl2↑)。
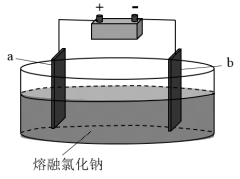
(6)通电时,C1-向___ (填“a”或“b”)电极移动,发生___ (填“氧化反应”或“还原反应”)。
(7)电解一段时间后,在两个电极上分别生成金属钠和氯气。写出生成金属钠的电极反应式:___ 。
I.在一定条件下,以CH4和H2O为原料,通过下列反应制备甲醇(CH3OH)。
已知:①CH4+H2O(g)
②CO(g)+2H2(g)
(1)反应②的正反应属于
(2)上述两个反应达到平衡后,在其它条件不变的情况下,通过减小容器体积增大压强,则化学平衡向逆反应方向移动的是
(3)在密闭容器中发生①反应,若CH4起始浓度为2.0mol·L-1,水蒸气起始浓度为3.0mol·L-1,反应进行5min后,测得CH4浓度为0.5mol·L-1,则v(CH4)=
Ⅱ.常温下,浓度均为0.1mol·L-1的两种溶液;①氨水②NH4Cl溶液。
(4)写出①氨水中NH3·H2O的电离方程式:
(5)测得②溶液的pH<7,则溶液中c(NH
Ⅲ.如图所示装置,用惰性电极电解熔融氯化钠(2NaCl

(6)通电时,C1-向
(7)电解一段时间后,在两个电极上分别生成金属钠和氯气。写出生成金属钠的电极反应式:
20-21高二上·福建泉州·期中
类题推荐
CO和H2可作为能源和化工原料,应用十分广泛。工业上可利用CO或CO2与H2反应来制备甲醇。
反应①:2H2(g)+CO(g) CH3OH(g)△H=-90.8kJ·mol-1
CH3OH(g)△H=-90.8kJ·mol-1
反应②:H2(g)+CO2(g) H2O(g)+CO(g)△H=+41.2kJ·mol-1
H2O(g)+CO(g)△H=+41.2kJ·mol-1
(1)写出用CO2与H2反应制备甲醇的热化学方程式______________ 。
(2)已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g) H2(g)+CO2(g),该反应平衡常数随温度的变化如表所示:
H2(g)+CO2(g),该反应平衡常数随温度的变化如表所示:
升高温度,该平衡的移动方向是______________ (填“正向”或“逆向”)。500℃时,CO和H2O的起始浓度均为0.020mol·L-1,该条件下CO的平衡浓度为:______________ mol·L-1。
(3)一定条件下,可以由CO2(g)和H2(g)合成CH4(g),同时还生成H2O(g)。向恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,10min达到平衡时部分物质的量浓度如图所示,该温度下的的平衡常数等于_______________ 。
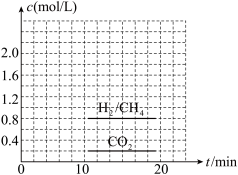
(4)若在20min时减小压强,并在30min时达到平衡状态,请在图2中画出H2的物质的量浓度随时间变化的图象__________________ 。

(5)工业上电解Na2CO3溶液可以生成NaHCO3和NaOH两种工业重要原料,装置如图所示。请写出阳极的电极反应式______________________ 。

反应①:2H2(g)+CO(g)
反应②:H2(g)+CO2(g)
(1)写出用CO2与H2反应制备甲醇的热化学方程式
(2)已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(3)一定条件下,可以由CO2(g)和H2(g)合成CH4(g),同时还生成H2O(g)。向恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,10min达到平衡时部分物质的量浓度如图所示,该温度下的的平衡常数等于

(4)若在20min时减小压强,并在30min时达到平衡状态,请在图2中画出H2的物质的量浓度随时间变化的图象

(5)工业上电解Na2CO3溶液可以生成NaHCO3和NaOH两种工业重要原料,装置如图所示。请写出阳极的电极反应式

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 CH3OH(g)
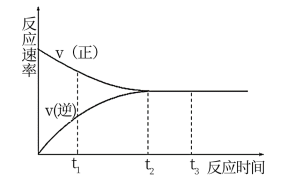
CH3OH(g) 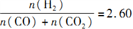 时体系中的CO平衡转化率(a)与温度和压强的关系如图所示。
时体系中的CO平衡转化率(a)与温度和压强的关系如图所示。


