填空题 适中0.65 引用1 组卷137
运用化学反应原理知识研究SO2与O2的反应对工业生产硫酸有重要意义。
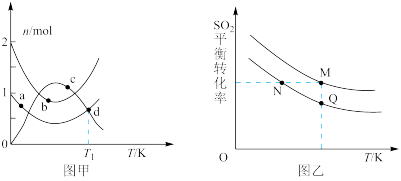
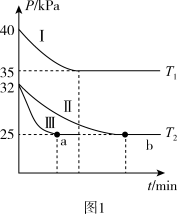
(1)向体积均为2L的恒容密闭容器中,分别加入2 mol SO2与1 mol O2,反应相同时间,不同温度下各容器中SO2、O2、SO3的物质的量如图甲所示。
①反应 一定条件下能自发进行的原因是
一定条件下能自发进行的原因是___________ 。
②图中a、b、c三点中处于平衡状态的是___________ 点。
③T1温度时反应的平衡常数为___________ 。
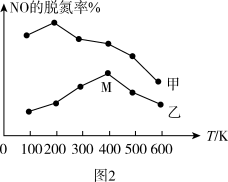
(2)若在两个体积相等的容器内起始分别加入2 mol SO2和1 mol O2、1 mol SO2和0.5 mol O2,SO2的平衡转化率随温度的变化如图乙所示。
①M、Q两点容器内压强p(M)___________ 2p(Q)
②M、N两点的平衡常数K (M)___________ K(N)
③M、N、Q三点的正反应速率v(M)正、v(N)正、v(Q)正由大到小的顺序是___________ 。

(1)向体积均为2L的恒容密闭容器中,分别加入2 mol SO2与1 mol O2,反应相同时间,不同温度下各容器中SO2、O2、SO3的物质的量如图甲所示。
①反应
②图中a、b、c三点中处于平衡状态的是
③T1温度时反应的平衡常数为
(2)若在两个体积相等的容器内起始分别加入2 mol SO2和1 mol O2、1 mol SO2和0.5 mol O2,SO2的平衡转化率随温度的变化如图乙所示。
①M、Q两点容器内压强p(M)
②M、N两点的平衡常数K (M)
③M、N、Q三点的正反应速率v(M)正、v(N)正、v(Q)正由大到小的顺序是
20-21高二上·江苏南通·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网