解答题-实验探究题 适中0.65 引用2 组卷460
无水碱式氯化铜[Cu2(OH)3Cl]为绿色或墨绿色结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。
Ⅰ模拟制备碱式氯化铜晶体
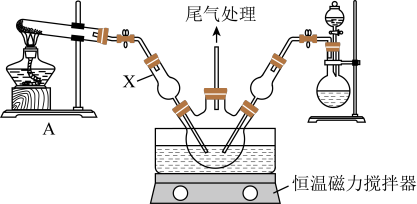
向精制的CuCl2溶液中通入NH3和HCl,调节溶液pH至5.0~5.5,控制反应温度为70~80℃,实验装置如图所示(部分夹持装置已省略)。
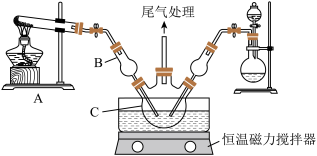
(1)仪器B为球型干燥管,其主要的作用是_____ 。装置C中的反应混合溶液pH过高或过低将导致产率降低,原因是_________ 。
(2)下列说法错误的是_____ 。
A.可通过观察装置C中的气泡速率,调节控制通入NH3和HCl的速率
B.可用pH计不断测定装置C中溶液的pH,以达到实验要求
C.可用右图装置吸收尾气,防止污染空气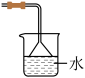
D.为了加快干燥速率,可选用加热烘干
(3)如图装置(活塞K处于打开状态),经过一系列操作获得较干燥的碱式氯化铜。请选择合适的编号,按正确的操作顺序补充完整.
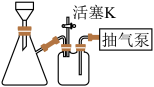
将反应产物冷却至40℃左右,倒入烧杯中→将滤纸放入布氏漏斗内,用蒸馏水润湿,打开抽气泵→( ) →( ) →( ) →( ) →用滤液淋洗烧杯,至所有晶体被收集到布氏漏斗中抽滤→( ) →( ) →( ) →确认抽干,开大活塞K,关抽气泵。
a.用倾析法转移溶液
b.加入洗涤剂
c.开大活塞K
d.微开活塞K
e.关活塞K
f.微关活塞K
g.待溶液快流尽时转移固体混合物
Ⅱ无水碱式氯化铜含量的测定
(4)上述操作后得到的固体经提纯得产品无水碱式氯化铜。称取产品加硝酸溶解,并加水定容至200mL,得到待测液。
采用银量法测定氯,用NH4SCN标准溶液滴定过量的AgNO3,发生反应Ag++SCN-=AgSCN↓,实验示意图如下。

(聚乙烯醇的作用是阻止AgCl与AgSCN的转化)
①滴定时,可选用NH4Fe(SO4)2作为指示剂,到达滴定终点的现象为_____ 。
②重复实验操作三次,消耗NH4SCN溶液体积平均为12.50mL。则称取的样品中n(Cl−)为_____ mol。
Ⅰ模拟制备碱式氯化铜晶体
向精制的CuCl2溶液中通入NH3和HCl,调节溶液pH至5.0~5.5,控制反应温度为70~80℃,实验装置如图所示(部分夹持装置已省略)。

(1)仪器B为球型干燥管,其主要的作用是
(2)下列说法错误的是
A.可通过观察装置C中的气泡速率,调节控制通入NH3和HCl的速率
B.可用pH计不断测定装置C中溶液的pH,以达到实验要求
C.可用右图装置吸收尾气,防止污染空气

D.为了加快干燥速率,可选用加热烘干
(3)如图装置(活塞K处于打开状态),经过一系列操作获得较干燥的碱式氯化铜。请选择合适的编号,按正确的操作顺序补充完整.

将反应产物冷却至40℃左右,倒入烧杯中→将滤纸放入布氏漏斗内,用蒸馏水润湿,打开抽气泵→
a.用倾析法转移溶液
b.加入洗涤剂
c.开大活塞K
d.微开活塞K
e.关活塞K
f.微关活塞K
g.待溶液快流尽时转移固体混合物
Ⅱ无水碱式氯化铜含量的测定
(4)上述操作后得到的固体经提纯得产品无水碱式氯化铜。称取产品加硝酸溶解,并加水定容至200mL,得到待测液。
采用银量法测定氯,用NH4SCN标准溶液滴定过量的AgNO3,发生反应Ag++SCN-=AgSCN↓,实验示意图如下。

(聚乙烯醇的作用是阻止AgCl与AgSCN的转化)
①滴定时,可选用NH4Fe(SO4)2作为指示剂,到达滴定终点的现象为
②重复实验操作三次,消耗NH4SCN溶液体积平均为12.50mL。则称取的样品中n(Cl−)为
2020·浙江·模拟预测
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网