单选题 适中0.65 引用1 组卷99
2SO2(g)+O2(g) 2SO3(g) △H=-196.6KJ/mol是制备硫酸的重要反应。下列关于该反应的叙述不正确的是
2SO3(g) △H=-196.6KJ/mol是制备硫酸的重要反应。下列关于该反应的叙述不正确的是
| A.反应达到平衡状态后,SO3(g)浓度保持不变 | B.催化剂V2O5能够提高SO2的平衡转化率 |
| C.增加O2的浓度有利于提高SO2的平衡转化率 | D.采用450℃高温可以缩短反应达到平衡的时间 |
20-21高二上·河南新乡·期中
类题推荐
下列关于反应2SO2(g)+O2(g)⇌2SO3(g)的描述正确的是
| A.使用催化剂,SO2的平衡转化率增大 |
| B.增大O2浓度,平衡常数K增大 |
| C.当2 |
| D.升高温度,反应物中活化分子百分数提高,反应速率增大 |
工业上制硫酸的一步重要的反应是SO2在400-500℃下催化氧化反应: 2SO2+O2 2SO3,该反应是个正反应放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中不正确的是
2SO3,该反应是个正反应放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中不正确的是
 2SO3,该反应是个正反应放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中不正确的是
2SO3,该反应是个正反应放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中不正确的是| A.使用催化剂的目的是加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.增加O2的浓度,可以提高SO2的转化率 |
| D.当SO2和SO3的浓度相等时,反应一定达到平衡 |
工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤:2SO2(g)+O2(g) 2SO3(g)。工业制硫酸的原理示意图:
2SO3(g)。工业制硫酸的原理示意图:
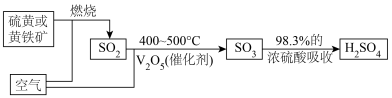
SO2的平衡转化率(%)随温度和压强的变化情况见下表:
下列说法不正确 的是

SO2的平衡转化率(%)随温度和压强的变化情况见下表:
温度/℃ | 平衡时SO2的转化率/% | ||||
0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
| A.使用催化剂可以缩短反应达到平衡所需的时间 |
| B.通常不采取加压措施是因为常压下SO2的转化率已相当高 |
| C.工业生产中通入过量的空气可以提高SO2的平衡转化率 |
| D.反应选择在400~500 ℃,主要是让V2O5的活性最大、SO2的平衡转化率提高 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


