解答题-工业流程题 适中0.65 引用1 组卷194
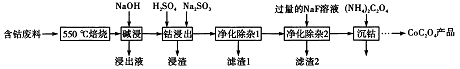
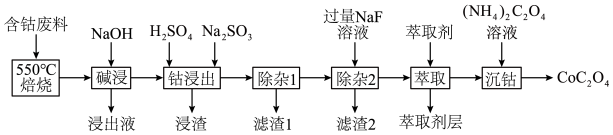
CoC2O4是制备金属钴的原料。利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
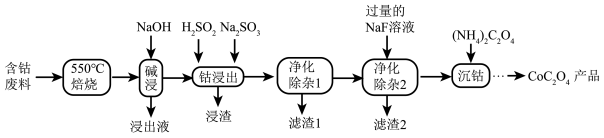
(1)“550℃煅烧”的目的是__________ 。
(2)“浸出液”的主要成分是________________ 。
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为__________ 。
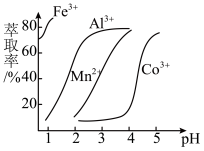
(4)“净化除杂1”过程中,需在40~50℃加入H2O2溶液,其目的是____________ (用离子方程式表示);再升温至80~85℃,加入Na2CO3溶液,调pH至5,“滤渣I”的主要成分是___________ 。
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×l0−5mol/L,则滤液中c(Mg2+)为____________ [已知Ksp(MgF2)=7.35×10−11、Ksp(CaF2)=1.05×10−10]

(1)“550℃煅烧”的目的是
(2)“浸出液”的主要成分是
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为
(4)“净化除杂1”过程中,需在40~50℃加入H2O2溶液,其目的是
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×l0−5mol/L,则滤液中c(Mg2+)为
19-20高二下·湖南常德·期中
类题推荐
草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分为 ,含少量
,含少量 、
、 、CaO、MgO、碳及有机物等)制取
、CaO、MgO、碳及有机物等)制取 的工艺流程如下:
的工艺流程如下:
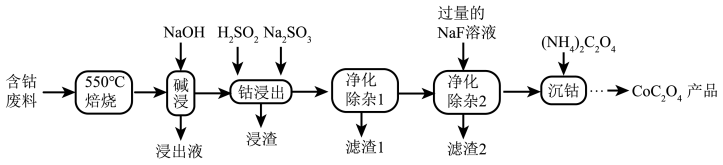
(1)“550℃焙烧”的目的是___________ 。
(2)“浸出液”的主要成分是___________ 。
(3)“钴浸出”过程中 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(4)“净化除杂1”过程中,先在40~50℃加入 ,其作用是
,其作用是___________ (用离子方程式表示);再升温至80~85℃,加入 溶液,调pH至4.5.加入
溶液,调pH至4.5.加入 时温度不宜过高的原因是:
时温度不宜过高的原因是:___________ ,加入 溶液时调pH至4.5的目的是:
溶液时调pH至4.5的目的是:___________ 。
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中 ,则滤液中
,则滤液中 为
为___________ 。[已知 、
、 ]。
]。

(1)“550℃焙烧”的目的是
(2)“浸出液”的主要成分是
(3)“钴浸出”过程中
(4)“净化除杂1”过程中,先在40~50℃加入
| 氢氧化物 | 开始沉淀时的pH | 沉淀完全时 pH (残留离子深度) | 沉淀开始溶解的pH | 沉淀完全溶解的pH | |
| 初深度 | |||||
| 6.6 | 7.6 | 9.2 | 14.1 | —— | |
| 9.4 | 10.4 | 12.4 | 14 | —— | |
| 1.5 | 2.3 | 4.1 | 14 | ||
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网