解答题-结构与性质 适中0.65 引用1 组卷122
已知四种短周期元素的原子序数的大小顺序为 ;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物
;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物 、
、 ,氢原子与B可形成两种共价化合物
,氢原子与B可形成两种共价化合物 、
、 。试回答下列问题:
。试回答下列问题:
(1)C元素的元素符号为_____ ;写出A的电子排布式______ 。
(2)写出D元素形成的 分子的结构式
分子的结构式____ ,其中 键与
键与 键的数目比为
键的数目比为______ 。
(3)B、D元素的第一电离能大小关系为:B_______ D(填“<”或“>”)。
(4) 对应的水化物的碱性比
对应的水化物的碱性比
______ (填“强”或“弱”);写出 的电子式
的电子式________ 。
(5)化合物 、
、 它们结构与组成相似,热稳定性更强的是
它们结构与组成相似,热稳定性更强的是__________ (填化学式), 的沸点比
的沸点比 高得多的原因是
高得多的原因是_______________ 。
(6)下列选项能作为C元素和氧元素非金属性强弱比较的依据的是_________ 。
a.C的氧化物对应的水化物的酸性弱于盐酸
b.C元素的电负性小于氯的电负性
c.化学反应:
(7)B和C可以形成化合物 ,
, 分子中空间结构为
分子中空间结构为___ (填“V型”成“直线型”)。中心原子C采用____ 杂化。
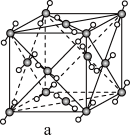
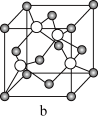
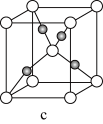
(8)元素B和铜原子形成的化合物 晶体结构可能是
晶体结构可能是______ (填字母)。
(1)C元素的元素符号为
(2)写出D元素形成的
(3)B、D元素的第一电离能大小关系为:B
(4)
(5)化合物
(6)下列选项能作为C元素和氧元素非金属性强弱比较的依据的是
a.C的氧化物对应的水化物的酸性弱于盐酸
b.C元素的电负性小于氯的电负性
c.化学反应:
(7)B和C可以形成化合物
(8)元素B和铜原子形成的化合物



20-21高三上·天津·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


